くも膜下出血はどんな訴えで来院するか
くも膜下出血の典型的な訴えは、「生涯で最悪の頭痛」や「雷鳴頭痛」と呼ばれる、突発的で激しい頭痛です。痛みが数秒から数分以内という短時間でピークに達するのが特徴で、しばしば嘔気・嘔吐、項部硬直、光過敏などを伴います。
しかし、必ずしも典型的な激しい頭痛のみで来院するわけではなく、意外な訴えで受診し、誤診のリスクとなるケースも多数報告されています。
■代表的な「意外な訴えや症状」は以下の通りです。
1. 軽度・非典型的な頭痛や首・肩の痛み
- 「なんだかいつもと違う」と自ら歩いて診察室に入ってくるような、比較的軽度な症状で来院することがあります。
- 「頭の中を風が吹き抜けるようだ」といった奇妙な表現で痛みを訴える患者もいます。
- 閃輝暗点を伴って発症し、単なる片頭痛と誤診されやすいケースもあります。また、緊張型頭痛として見過ごされることもあります。
- 首や肩の痛みとして現れ、頸椎症候群(肩こりやむち打ちのような症状)と診断されてしまうこともあります。
- 本出血の数週間前に起こる少量の出血による「警告頭痛」が、一般的な頭痛として見逃されるケースも多くあります。
2. 循環器系の症状
- くも膜下出血は発症時の急激なストレス(カテコラミンサージ)を引き起こし、心電図異常(ST変化や陰性T波、不整脈)や「たこつぼ型心筋症」を高頻度で合併します。
- そのため、頭痛よりも心不全症状が前面に出たり、急性心筋梗塞や致死性不整脈と診断され、循環器科に回されてしまうことがあります。
3. 消化器系の症状
- 激しい嘔気・嘔吐を主訴に来院し、胃腸炎などの消化器疾患と誤診されることがあります。中には、嘔気・嘔吐を理由に上部消化管内視鏡検査を実施された後に、くも膜下出血が判明したケースも報告されています。
4. 失神や意識障害
- 「失神」や「意識障害」を主訴に救急搬送されるケースも少なくありません。詳細な問診を行わないと、単純な心血管性失神、起立性失神、あるいはてんかんなどの痙攣発作と誤認される危険性があります。
5. めまいや眼の症状
- 回転性または浮動性の「めまい」を訴える患者もいます。
- くも膜下出血に伴って硝子体出血(テルソン症候群)などを起こし、視力障害や急性緑内障などの眼科疾患と鑑別が必要になるケースもあります。
このように、くも膜下出血は単なる「激しい頭痛」にとどまらず、風邪、消化器疾患、循環器疾患、一次性の頭痛などに類似した多岐にわたる訴えで来院することがあるため、注意深い病歴聴取が求められます。
くも膜下出血の誤診
くも膜下出血はどのような病名で誤診されているか、を示した論文をご紹介します。
Edlow, Jonathan A., and Louis R. Caplan. “Avoiding Pitfalls in the Diagnosis of Subarachnoid Hemorrhage.” New England Journal of Medicine 342, no. 1 (2000): 29–36. https://doi.org/10.1056/NEJM200001063420106.
初診時の誤診率
4つの研究の統合データによると、くも膜下出血の患者685例中220例、すなわち全体の32%が初診時に誤診されていました。 なお、個別の研究を見ると、誤診率は23〜37%とするもの、25%とするもの、あるいは50%に上るとする報告があり、研究によってばらつきがあります。
誤診病名の内訳(%)
誤診された220例における、具体的な誤診病名とその割合は以下の通りです(※一部の患者は複数の診断を受けているため、各項目の割合を足しても100%にはなりません)。
- 診断がつかない、または原因不明の頭痛:24% (52例)
- 片頭痛、群発頭痛、または緊張型頭痛:21% (47例)
- 髄膜炎または脳炎:10% (23例)
- 全身性感染症(インフルエンザ、胃腸炎、ウイルス症候群など):10% (23例)
- 脳卒中または脳虚血:8% (17例)
- 高血圧クリーゼ(高血圧緊急症):7% (16例)
- 心疾患(心筋梗塞、不整脈、失神など):6% (14例)
- 副鼻腔関連疾患:6% (13例)
- 頸部の問題(椎間板関連または関節炎):5% (11例)
- 精神科的診断(詐病やアルコール中毒を含む):5% (10例)
- 外傷関連疾患:1% (3例)
- 背部痛(背中の痛み):1%未満 (1例)
- その他:15% (32例)
このように、最も多い誤診は「原因不明の頭痛」や「一次性頭痛(片頭痛など)」ですが、風邪や胃腸炎、さらには高血圧や心疾患など、頭痛以外の症状やバイタルサインの異常に気を取られて誤診されているケースも少なくないことがわかります。
検査
血液検査所見
くも膜下出血そのものを直接診断できるような特異的な血液検査所見はありません。SAHの確定診断は、頭部CTやMRIなどの画像検査、および腰椎穿刺による髄液検査によって行われます。
しかし、SAHの発症に伴う脳への強いダメージや急激なストレス(カテコラミンサージ)によって、二次的に引き起こされる特徴的な血液検査の異常所見はいくつか存在します。主なものは以下の通りです。
1. 心筋マーカーの上昇(トロポニン、CK-MB)
- SAHが発症すると、交感神経の急激な興奮(カテコラミンサージ)により「たこつぼ型心筋症」をはじめとする心筋障害を合併することがあります。
- これに伴い、血液検査で血中トロポニン(トロポニンTなど)やクレアチンキナーゼ(CK-MB)の上昇がみられることがあります。このような所見や心電図異常は、25〜35%の患者で観察されると報告されています。
2. 電解質異常(低ナトリウム血症、低カリウム血症)
- SAHなどの重症な脳損傷が起こると、「脳性塩類喪失症候群(CSW)」や「抗利尿ホルモン分泌不適切症候群(SIADH)」を引き起こしやすくなります。
- これにより、血清ナトリウムやカリウムの低下がみられることがあり、このような不可解な電解質異常自体がSAHの存在を示唆する手がかりの一つになることがあります。
3. 血糖値の上昇やカリウム低下(EMERALD SAHルールにおける指標)
- 上でも触れた、救急外来でSAHをスクリーニングするための「EMERALD SAHルール」には、血液検査の項目が含まれています。
- 具体的には、「血糖値 > 115 mg/dL」および「血清カリウム < 3.9 mEq/L」が、血圧高値(収縮期150超・拡張期90超)と並んでSAHを疑う陽性基準として設定されています。
画像検査
私自身、以下のようなフローチャートに沿って画像検査を行っています。
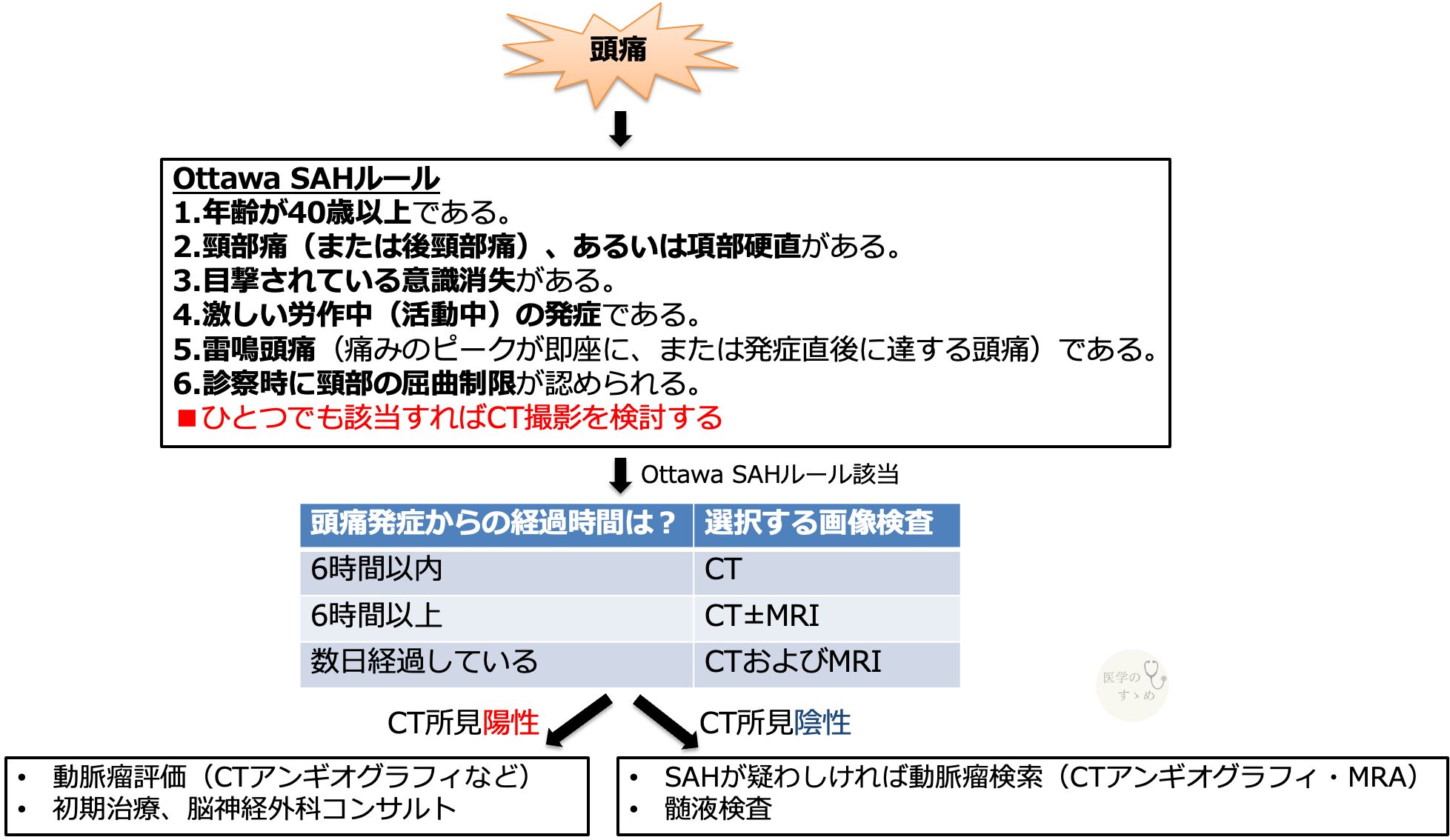
CTを行うかの判断基準
CTの感度は、出血量(重症度)と発症からの経過時間によって大きく変化します。脳脊髄液の循環や自然溶解によって血液が吸収されていくため、時間が経つほど感度は低下します。
- 発症6時間以内⇢感度・特異度ともにほぼ100%
- 発症12時間以内⇢感度 98〜100%
- 発症24時間以内⇢感度 約93%
- 発症5日後⇢感度 85%
- 発症6日後⇢感度57~85%
このように、発症から日数が経過している場合、CTの感度は著しく低下するため、CTで異常が見られなくても腰椎穿刺などによる追加確認が推奨されます。
Ottawa SAHルール
- 年齢が40歳以上である。
- 頸部痛(または後頸部痛)、あるいは項部硬直がある。
- 目撃されている意識消失がある。
- 激しい労作中(活動中)の発症である。
- 雷鳴頭痛(痛みのピークが即座に、または発症直後に達する頭痛)である。
- 診察時に頸部の屈曲制限が認められる。
■ひとつでも該当すればCT撮影を検討する
■いずれの項目も満たさない場合は、SAHの可能性は低いと判断し、除外することが可能
このルールは、16歳以上で意識が清明であり、非外傷性の急性頭痛(痛みのピークが1時間以内)を訴え、かつ明らかな神経学的異常所見がない患者を見極めるためのツールとして用いられます。
これら6項目のうち1つでも当てはまる場合は、くも膜下出血の可能性を否定できず、頭部CTなどの精査を行う必要があります。逆に、いずれの項目も満たさない場合は、SAHの可能性は低いと判断し、除外することが可能です。
ただし、すでに神経学的異常所見がある場合や、過去に脳動脈瘤やくも膜下出血の既往がある場合、脳腫瘍を指摘されている場合、あるいは同様の頭痛を過去6カ月以上の期間内に3回以上繰り返している患者に対しては適応外となります
EMERALD SAHルール
Ottawa SAHルールの特異度の低さを改善する目的などで、2016年に日本の研究(国立国際医療研究センター病院など)によって報告された新しい基準です。Ottawa SAHルールが「陽性」となった場合に、さらに評価を進める指標として用いられることもあります。
- 収縮期血圧 > 150 mmHg
- 拡張期血圧 > 90 mmHg
- 血糖値 > 115 mg/dL
- 血清カリウム < 3.9 mEq/L
■4項目のうち一つでも当てはまれば「陽性」となり、CT撮像が推奨されます。
【欠点】
- 依然として特異度が低い: 日本の多施設前向きコホート研究では感度100%を達成しましたが、特異度は14.5%にとどまっており、Ottawaルールよりわずかに改善したものの、依然として偽陽性が多く不要なCTを劇的に減らすには至っていません。
- 外部検証の不足と感度の低下リスク: イギリスのコホートを用いた外部検証では、特異度は27%でしたが、感度が81%に低下してしまった(=くも膜下出血の患者を2割弱見逃してしまう)ことが報告されており、まだ外部検証が十分ではないという課題があります(Foley et al. Clin Med (Lond). 2021.PMID: 33762366)。
OttawaルールとEMERALDルールの使い分け
- Ottawaルールは「CTを撮らなくてもよい患者を見つける(除外する)」ための最初の網として使います。
- EMERALDルールは「Ottawaルールで引っかかった患者の中から、本当にCTを撮るべき患者を客観的数値(血圧・採血)で絞り込む」ための2番目の網として使います。
※注意点 EMERALDルールを用いても特異度は依然として低く、偽陽性(SAHではないのに陽性となること)は多く存在します。そのため、これらのルールはあくまで補助ツールとして使用し、「いつもと違う頭痛」や「発症状況が不自然」といった臨床的な直感がある場合は、ルールにとらわれず、CT検査の閾値を下げて画像評価を行うことが重要です。
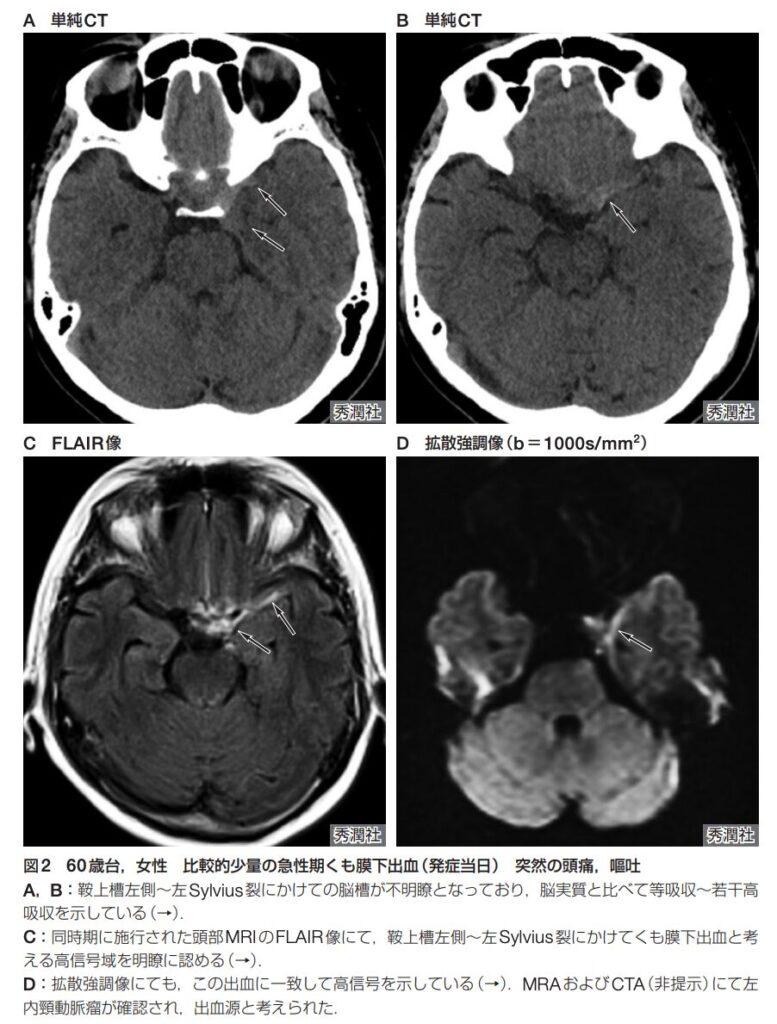
CT画像の特徴
正常解剖と典型的なCT画像の特徴
まずは正常解剖からおさらいです。
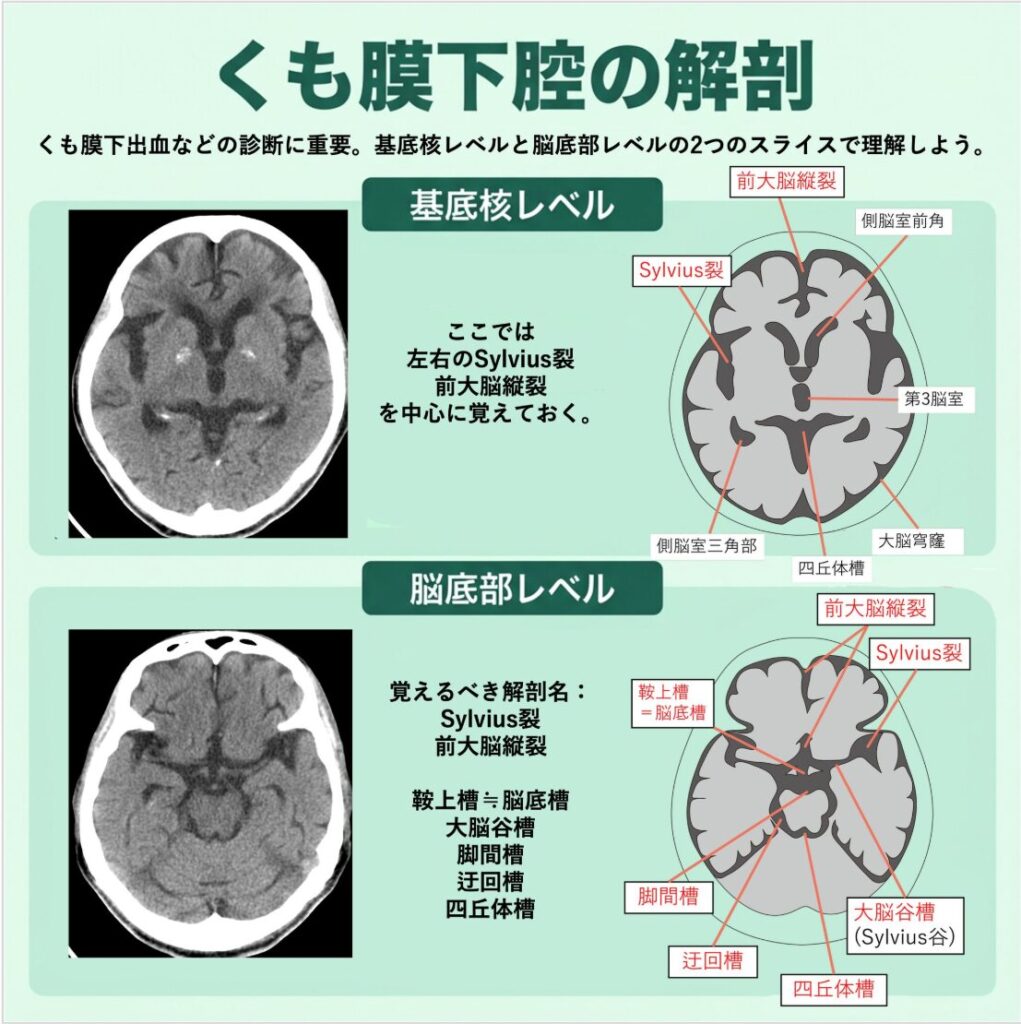
見逃さないための読影のポイント
典型的なSAHの場合、頭部単純CTにおいて、脳の底部にある「鞍上槽」を中心として、前大脳縦裂、両側のシルビウス谷・裂、橋前槽、迂回槽へと血液由来の高吸収領域が広がり、いわゆる「ペンタゴン(五角形)」の形状を示します。このような典型例であれば診断は容易です。
少量の出血や、発症から時間が経過して血液の吸収値が低下している場合は、診断が困難になり見逃しの原因となります。 見逃しを防ぐためには、単に「白く光る高吸収域を探す」だけではなく、以下の視点で読影することが重要です。
- 左右差を比較する
- 脳槽や脳溝が、正常な脳脊髄液の吸収値(黒く抜ける状態)を示しているか?
- 脳槽や脳溝が不明瞭になっている部位はないか?
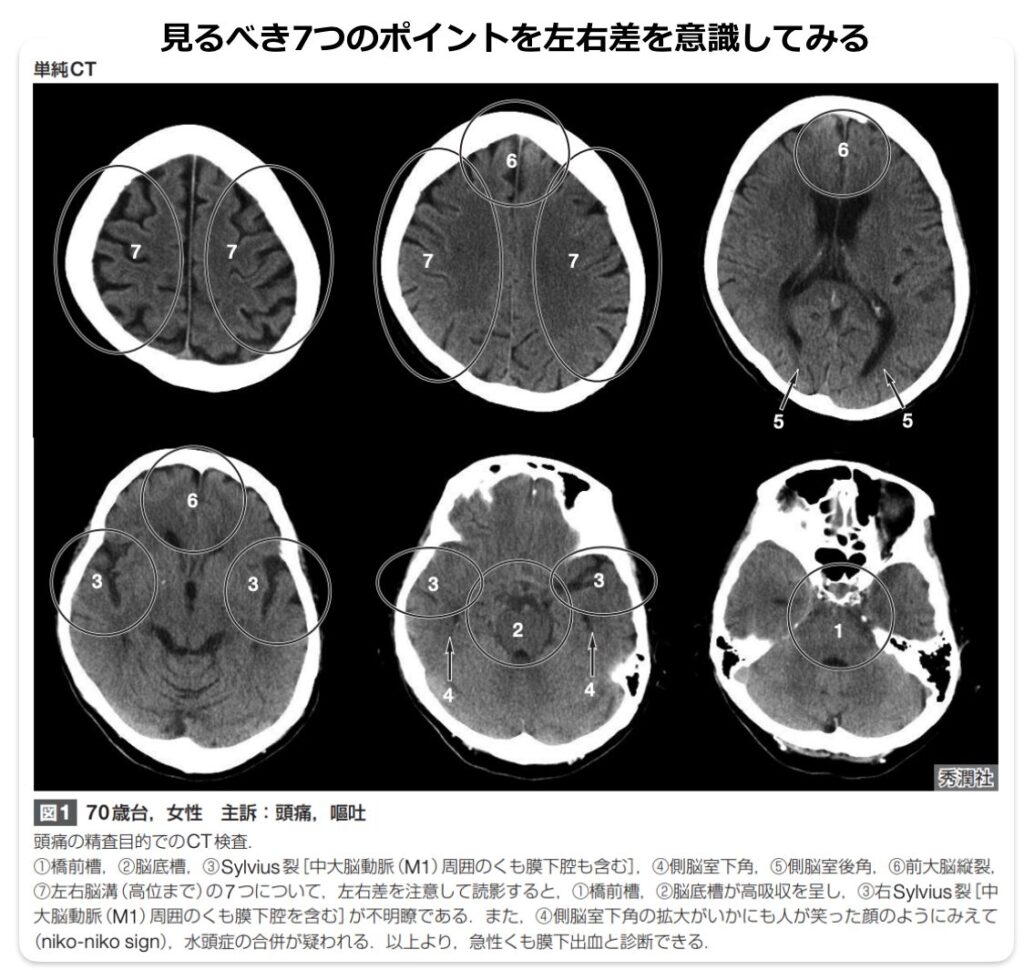
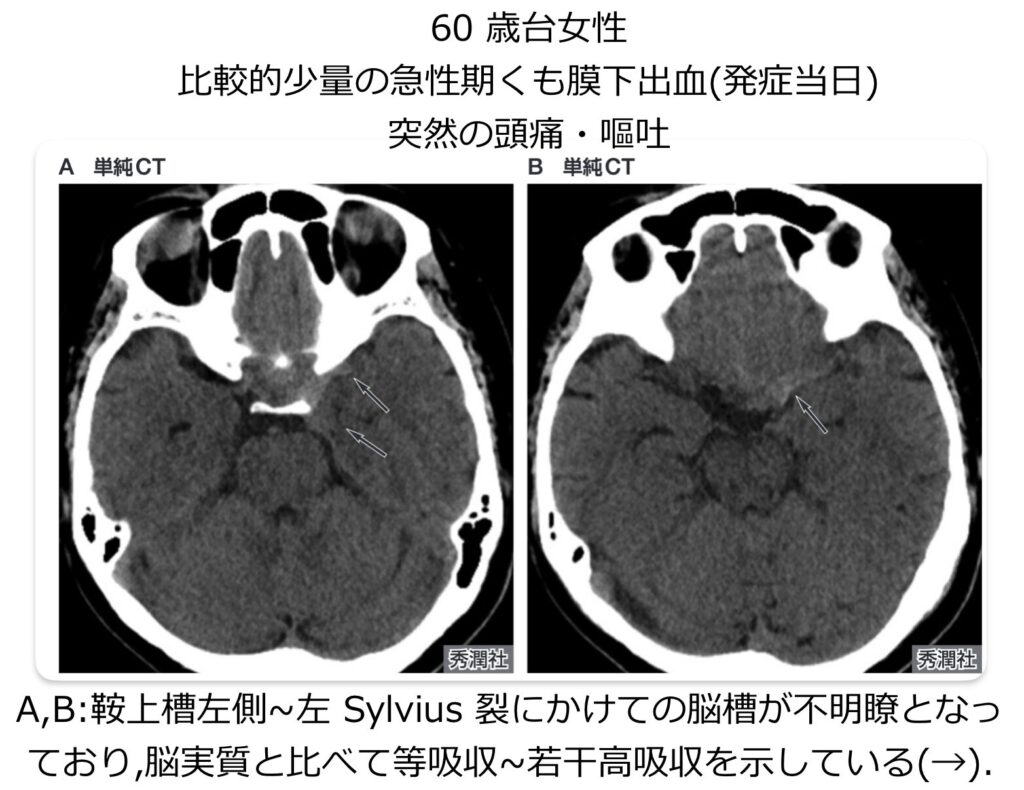
SAHを疑う「間接所見」
■出血そのものが分かりにくい場合でも、以下の特徴的な所見がSAHの存在を示唆する重要な手がかりになります。
- niko-niko sign: SAHの15〜30%に水頭症が合併します。特に両側の側脳室下角の拡大が最も早期に観察されやすく、これがCT上で「微笑んだ時の表情」に似ていることから「niko-niko sign」と呼ばれます。
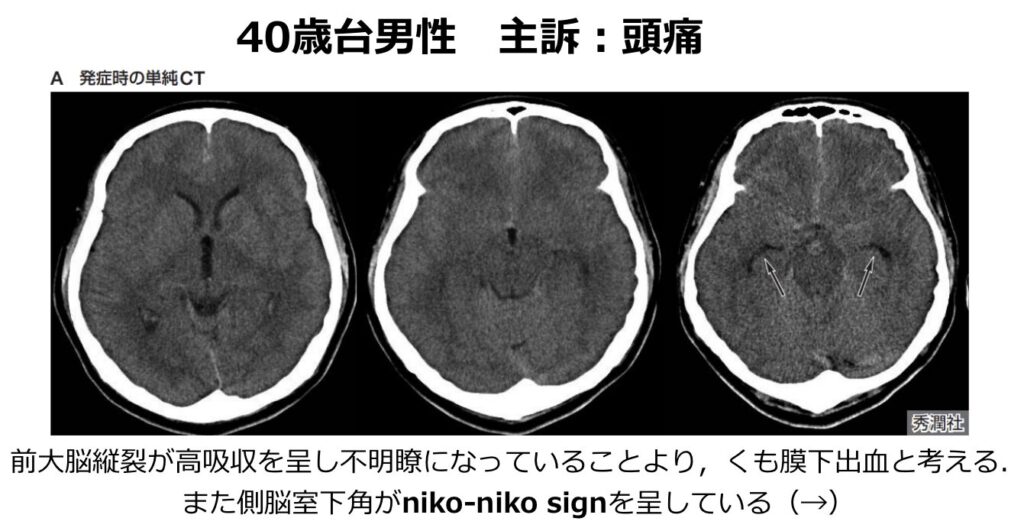
- 脳室内の液面像: 脳室内へ逆流した少量の出血が、側脳室後角に血液と髄液の「液面像」を伴って認められることがあり、これもSAHを示唆する重要な二次的所見です。
■CT画像の所見から、どの動脈瘤が破裂したのかをある程度予測することができます。
- 出血の分布による推測:
- 内頸動脈瘤: 破裂側の鞍上槽やシルビウス谷に出血が多く、シルビウス裂などに広がります。
- 中大脳動脈瘤: 破裂側のシルビウス裂を中心に出血することが多いです。
- 前交通動脈瘤: 前大脳縦裂下部を中心に、左右対称性に分布することが多いです。
- 椎骨脳底動脈瘤: 後頭蓋窩(脳幹周囲)を主体に出血し、高率に第四脳室に逆流します。
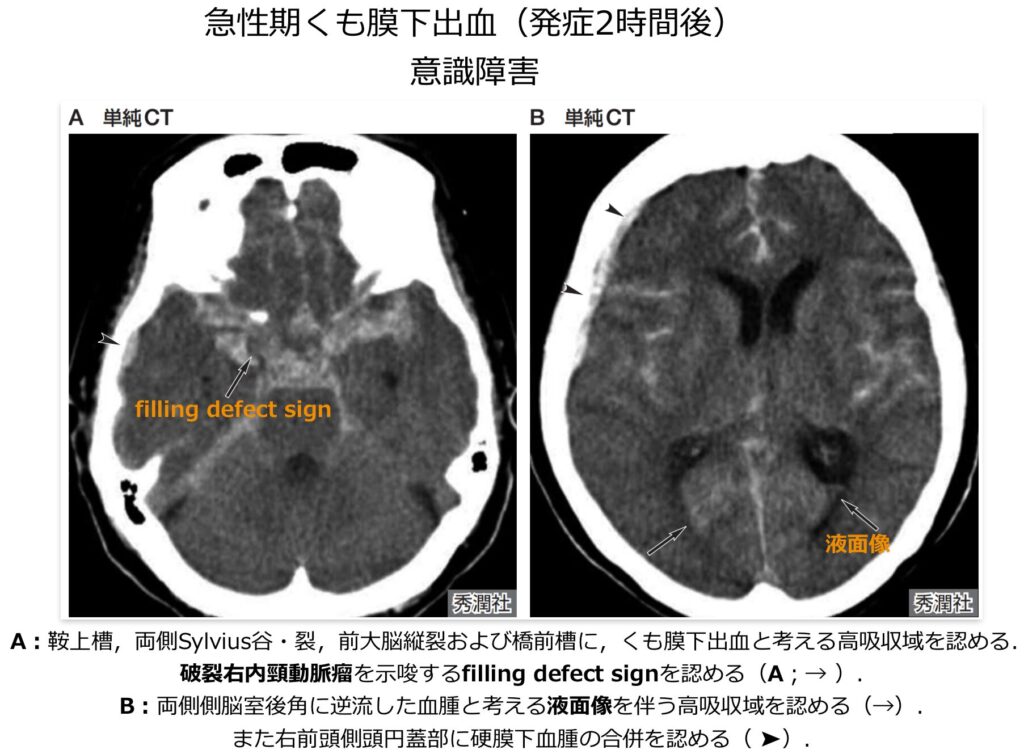
- filling defect sign(陰影欠損サイン): 比較的厚みのあるくも膜下出血の白い領域の中に、破裂した動脈瘤そのものを反映した「相対的な低吸収域(やや黒く抜けた部分)」が観察されることがあり、これをfilling defect signと呼びます。
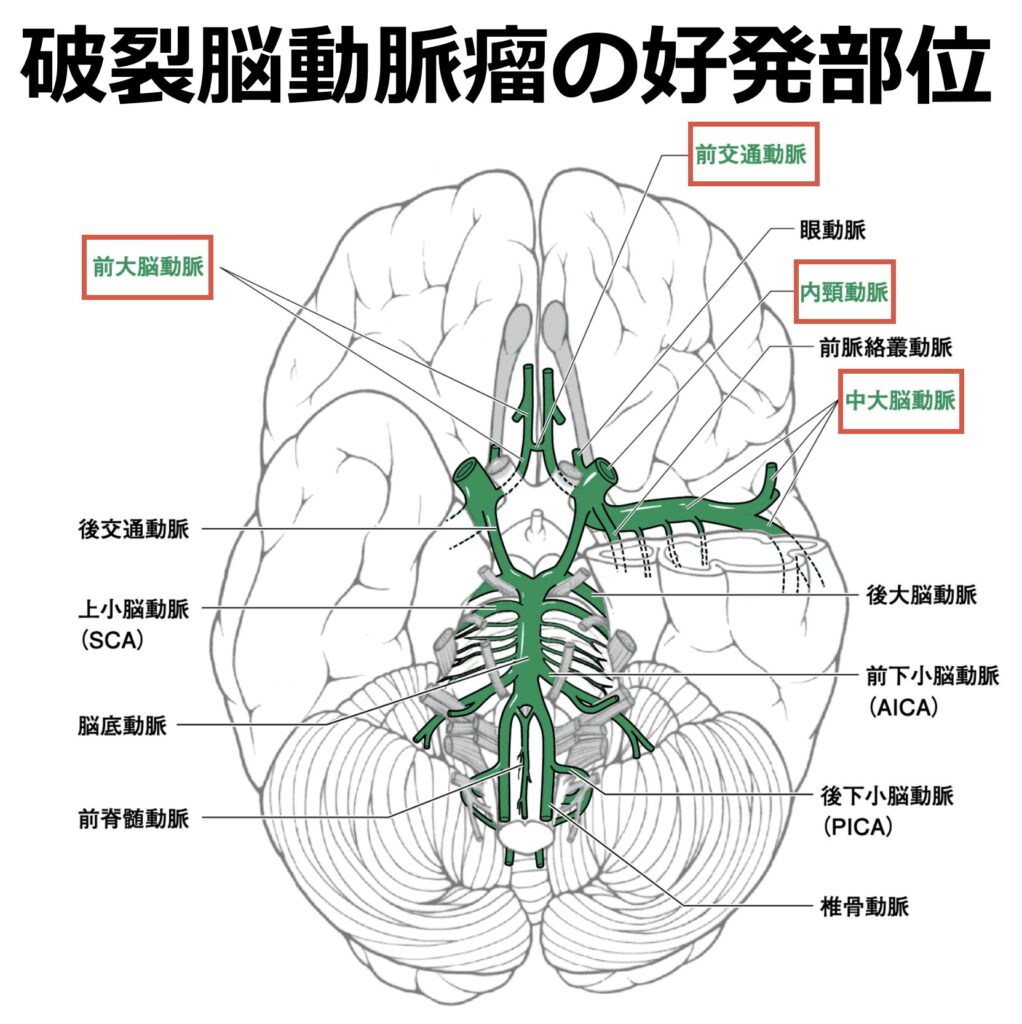
脳動脈瘤の好発部位
破裂脳動脈瘤の一般的な好発部位と発生の割合は、以下の通りです。
- 前大脳動脈に関連する動脈瘤(前交通動脈瘤や末梢性前大脳動脈瘤など):38%
- 中大脳動脈瘤:27%
- 内頸動脈瘤:26%
- 椎骨・脳底動脈瘤:9%
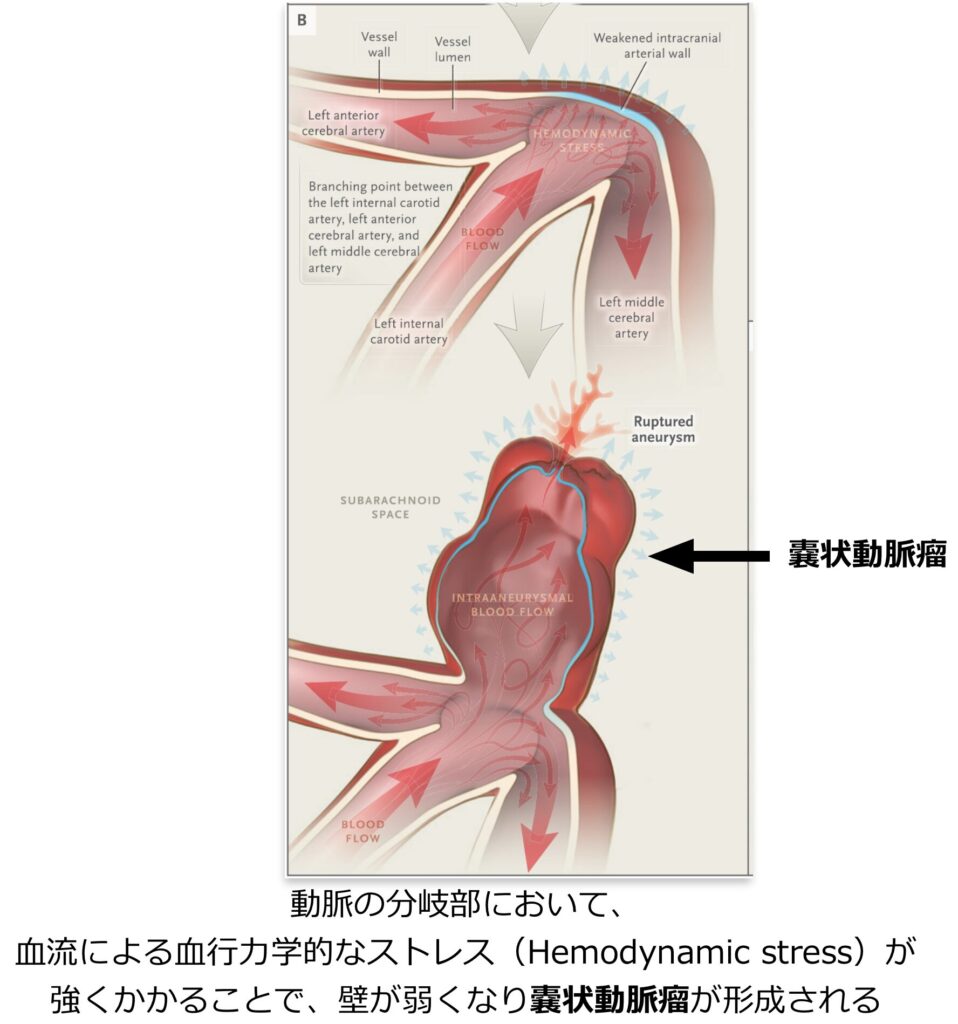
また、脳動脈瘤自体は、血流による血行力学的なストレスがかかりやすい頭蓋内動脈の分岐部に形成されやすいという特徴があります。
MRI
- 単純CTでSAHがはっきりしない場合や、発症から日数が経過している場合には、MRI(特にFLAIR像)が有用です。通常は髄液で黒く抜ける脳溝内に、FLAIR像で高〜等信号が見られればSAHの可能性が高いです(ただし、FLAIRでくも膜下腔が高信号を呈する病変・病態があります。詳しくは、「画像診断まとめ」様の「クモ膜下出血(SAH)のMRI画像診断(特にFLAIR) をご参照ください)。
時期別のMRIの感度
- 急性期(発症4〜5日まで):
- FLAIR像の感度は81〜100%。
- T2*強調像の感度は90.9〜94%。
- 急性期はFLAIR像が特に有用です。
- 亜急性期(発症5日〜14日):
- 時間経過とともにFLAIR像の感度は低下する(33.3〜75%になる)とする報告がある一方で、発症4日以降14日目までFLAIR像の感度が100%であるとする報告もあります。
- T2強調像は、亜急性期になると感度が100%に上昇(または高く維持)すると報告されており、FLAIR像に加えてT2強調像を撮像する必要があります。
MRIの留意点
MRIは有用なツールですが、完全ではありません。以下の点に注意が必要です。
- 腰椎穿刺の完全な代用にはならない: CTで検出できないレベルの微量な出血は、FLAIR像でも検出が難しいケース(偽陰性)が報告されており、画像検査のみでSAHを完全に除外することはできません。
- FLAIR像の偽陽性(特異度の低下要因): SAH以外の要因(髄膜炎、急性期脳梗塞、静脈血栓症、もやもや病、高濃度酸素投与、プロポフォールによる静脈麻酔など)でも、脳溝が高信号を示すことがあります。また、脳底槽では脳脊髄液の拍動によるゴーストアーチファクトが生じやすいため、読影には注意が必要です。
- T2*強調像の欠点: 出血の検出には優れていますが、その出血が今回の新しいものか、過去の古いものかの判別が難しい場合があります。
髄液検査
臨床的にくも膜下出血を強く疑うが CT や MRI が陰性の場合には,腰椎穿刺を検討します。腰椎穿刺でキサントクロミーの有無を確認します。キサントクロミーは、臨床的にくも膜下出血(SAH)を強く疑うものの、CTやMRIで陰性(異常なし)となった場合の診断において非常に有用です。
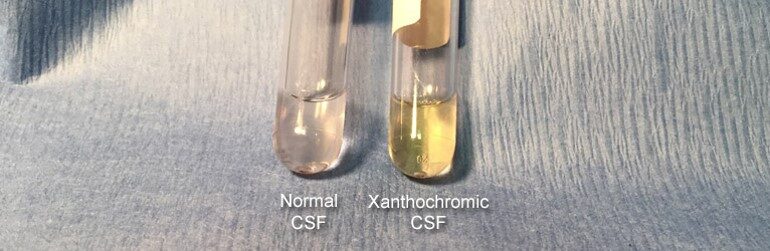
キサントクロミーの感度特異度・尤度比
Acad Emerg Med. 2016 Sep;23(9):963-1003. (PMID:2730647)によると、キサントクロミーの診断精度は以下の通り報告されています。
1. 分光光度計による測定(U.K. NEQASアルゴリズムを使用した場合)
- 感度: 100%
- 特異度: 95%
- 陽性尤度比(LR+): 15.23
- 陰性尤度比(LR-): 0.13
2. 肉眼での観察
- 感度: 85%
- 特異度: 97%
- 陽性尤度比(LR+): 24.67
- 陰性尤度比(LR-): 0.22
これらのデータから、以下のような検査の特性がわかります。
- 分光光度計による測定は、感度が100%と非常に高く、陰性尤度比も低いため、SAHを見逃さない(除外診断を行う)ツールとして非常に優れています。
- 肉眼での観察は、分光光度計に比べると感度が劣るリスクやばらつきがありますが、特異度(97〜98%)と陽性尤度比が非常に高いため、肉眼で変色が確認できた場合には、SAHの存在を強力に裏付ける(rule inする)所見として極めて有用です。
ただし、髄液検査においてキサントクロミーを評価する際は、以下の点に注意する必要があります。
- 適切なタイミングでの検査
- キサントクロミーが髄液中に出現するには、発症後4〜12時間程度の経過が必要です。発症直後に検査を行うと偽陰性となってしまうため注意が必要です。
- なお、一度出現すればその後2週間は陽性が持続します。
- 外傷性穿刺(Traumatic tap)との鑑別
- 髄液中の赤血球数(RBC > 1,000/μL)もSAHの指標(感度76%、特異度88%)となりますが、針を刺した際に出血が混入する外傷性穿刺によっても、9〜14%の確率でRBC > 1,000/μLとなってしまいます。そのため、キサントクロミーの有無を確認することが、手技による出血か、真のくも膜下出血かを鑑別するために重要です。
- 髄液初圧の測定
- SAH以外の雷鳴頭痛の原因疾患(低髄圧症候群や静脈洞血栓症など)では、頭蓋内圧の異常を伴います。
- そのため、髄液検査を行う際はキサントクロミーの確認だけでなく、必ず「初圧」を測定して評価することが鑑別診断において忘れてはならないポイントです。
キサントクロミーが生じるメカニズム
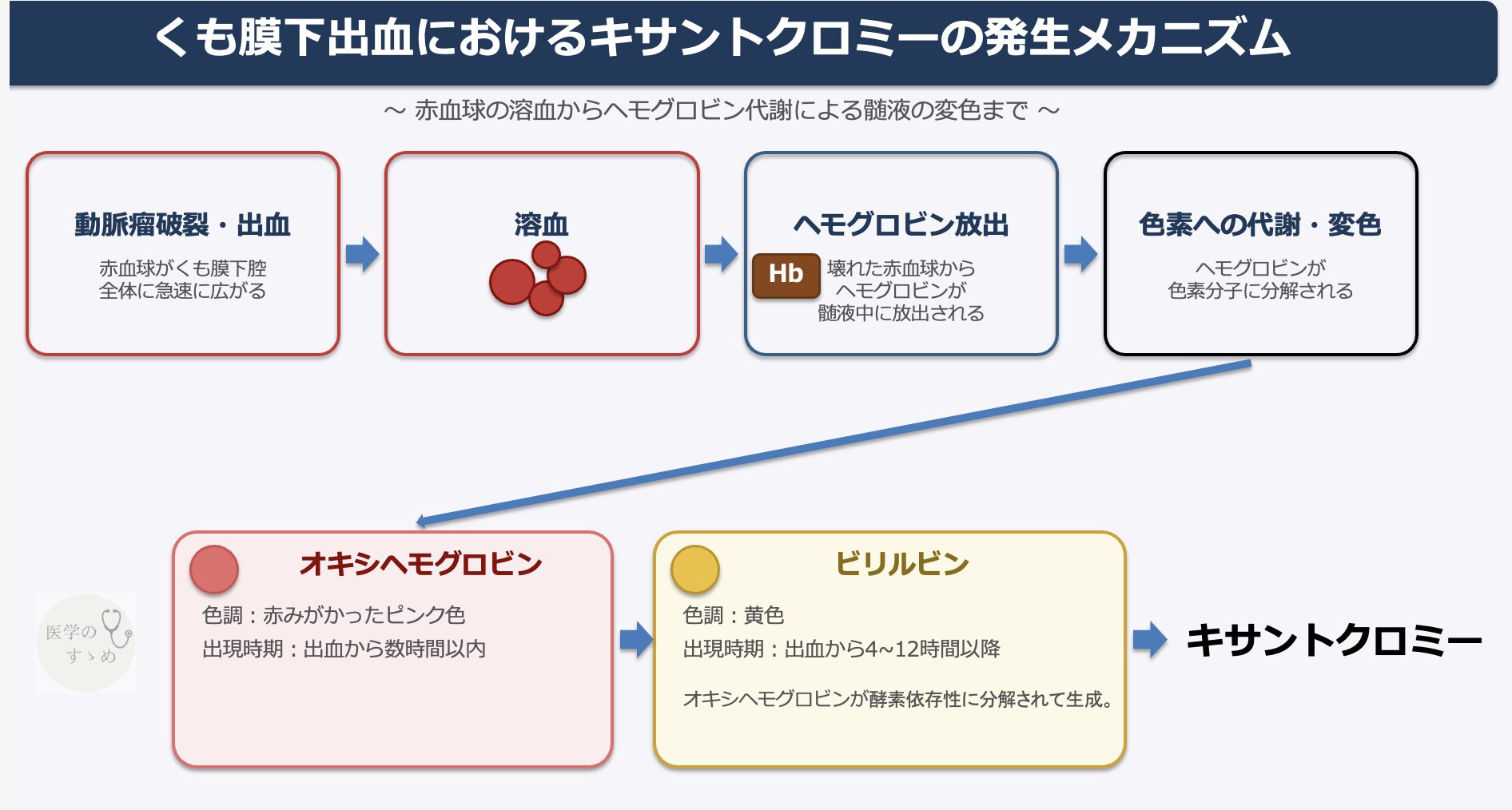
キサントクロミーが起きる理由は、くも膜下腔に流れ出た赤血球が髄液の中で壊れ、その成分が色素に変化するからです。
具体的には、以下のようなメカニズムで発生します。
- 出血と溶血: 動脈瘤が破裂すると、赤血球がくも膜下腔全体に急速に広がります。これらの赤血球は数日から数週間にわたって髄液中にとどまり、徐々に溶血していきます。
- ヘモグロビンの放出: 赤血球が壊れると、その中からヘモグロビンが髄液中に放出されます。
- 色素への代謝: 放出されたヘモグロビンは代謝され、色素を持った別の分子へと変化していきます。
- オキシヘモグロビン(赤みがかったピンク色): 出血から数時間以内に検出されるようになります。
- ビリルビン(黄色): オキシヘモグロビンが酵素の働きによって分解されると、黄色のビリルビンになります。
このように、赤血球から放出されたヘモグロビンが「オキシヘモグロビン」や「ビリルビン」といった色素に分解・代謝されることで、キサントクロミーが引き起こされます。
救急外来におけるくも膜下出血の急性期対応
「いかに再破裂を防ぐか」が最大の目標となります。
死亡率と再破裂率
- 30日後までの死亡率: 45%と報告されています。
- 24時間以内の再破裂率: 9〜17%(4〜14%とする報告もあります)。
- 再破裂患者の死亡率: 再破裂を起こした70%は死亡すると報告されています
疼痛コントロールと鎮静
激しい痛みや不安・興奮は血圧上昇を招き、再破裂のリスクを高めるため、積極的な介入が必要です。
- 鎮痛:フェンタニル
- 鎮静:プロポフォールやミダゾラム、また鎮痛・鎮静作用のあるデクスメデトミジンの持続投与を行います。
- 安静:
- 環境の調整: 患者の不安を取り除くため、可能な限り部屋を少し暗くし、静かな環境を保ちます。
- 刺激を少なくする: CT検査で確定診断がついた際、「急がなければ!」と慌ててストレッチャーで振動などの刺激を与えてしまうのは悪手です。物理的な刺激を加えることで院内で再破裂を起こす恐れがあるため、なるべく刺激を与えずに救急室に戻すよう細心の注意を払います。
血圧コントロール
- 降圧目標: 収縮期血圧を160 mmHg未満、または平均動脈圧(MAP)を110 mmHg未満にコントロールすることが日本のガイドライン等で推奨されています。しかし、再破裂例の多くがSBP 120〜140 mmHgで発生しているというデータから、それ以下(120〜140 mmHg未満)を目標に降圧することが妥当とする見解もあります。
- 使用薬剤: ニカルジピンなどのカルシウム拮抗薬の持続投与が一般的です。
ニカルジピン(ペルジピン®)1~2 mg を iv 後,2 mg/hrで開始します。
静脈炎が起きやすいので生食で希釈します。また配合変化あり基本単独ルートで投与します。
- 注意点: くも膜下出血の重症例では頭蓋内圧が亢進しています。この状態で急激かつ過度な降圧を行うと、脳灌流圧が低下し、致命的な脳虚血を引き起こす危険があるため、神経学的所見やバイタルを厳密に観察しながらコントロールをします。
参考文献
- Ois A, Vivas E, Figueras-Aguirre G, Guimaraens L, Cuadrado-Godia E, Avellaneda C, Bertran-Recasens B, Rodríguez-Campello A, Gracia MP, Villalba G, Saldaña J, Capellades J, Fernández-Candil JL, Roquer J. Misdiagnosis Worsens Prognosis in Subarachnoid Hemorrhage With Good Hunt and Hess Score. Stroke. 2019 Nov;50(11):3072-3076. doi: 10.1161/STROKEAHA.119.025520. Epub 2019 Oct 10. PMID: 31597551.
- 宍戸 肇,河北 賢哉.「脳卒中の基本知識を整理する」Beyond ER Vol.2 No.5 2023
- Lawton, Michael T., and G. Edward Vates. “Subarachnoid Hemorrhage.” New England Journal of Medicine 377, no. 3 (2017): 257–66.
- 松木 充「疾患別 急性くも膜下出血を見落とさないためのコツは何ですか?くも膜下出血をみつけたら直ちにどうすべきですか?」画像診断 Vol.35 No.10 2015
- 篠原 祐樹ら,「脳動脈瘤とくも膜下出血を究める くも膜下出血のCT・MRI診断」画像診断 34巻13号 (2014年10月発行)
- 宍戸 肇,河北 賢哉.「脳卒中の基本知識を整理する」Beyond ER Vol.2 No.5 2023
- https://xn--o1qq22cjlllou16giuj.jp/archives/13605 (2026/03/06閲覧)
- Edlow JA, Caplan LR. Avoiding pitfalls in the diagnosis of subarachnoid hemorrhage. N Engl J Med. 2000 Jan 6;342(1):29-36. doi: 10.1056/NEJM200001063420106. PMID: 10620647.
- https://scvmcmed.com/2017/03/13/am-report-022317-subarachnoid-hemorrhage/ (2026/03/08閲覧)
- Carpenter CR, Hussain AM, Ward MJ, Zipfel GJ, Fowler S, Pines JM, Sivilotti ML. Spontaneous Subarachnoid Hemorrhage: A Systematic Review and Meta-analysis Describing the Diagnostic Accuracy of History, Physical Examination, Imaging, and Lumbar Puncture With an Exploration of Test Thresholds. Acad Emerg Med. 2016 Sep;23(9):963-1003. doi: 10.1111/acem.12984. Epub 2016 Sep 6. PMID: 27306497; PMCID: PMC5018921.
- Claassen J, Park S. Spontaneous subarachnoid haemorrhage. Lancet. 2022 Sep 10;400(10355):846-862. doi: 10.1016/S0140-6736(22)00938-2. Epub 2022 Aug 16. PMID: 35985353; PMCID: PMC9987649.



コメント