どのような主訴でやってくるか
一見すると糖尿病とは関係なさそうな症状で来院することがあります。
• 「しゃべりにくい」
◦ 脳梗塞による構音障害のように見えますが、高度の脱水で口の中が乾燥して喋れなくなっているケースです(劇症1型糖尿病によるDKAなどで見られます)。
• 「お腹が痛い」「吐いた」「吐血した」
◦ DKAでは腹痛や悪心・嘔吐が非常に高頻度(約40〜50%)に見られます。激しい嘔吐を繰り返した結果、マロリー・ワイス症候群)をきたし、それを主訴に搬送されることもあります。
• 「右手が勝手に動く」「ぴくつく」
◦ これは糖尿病性舞踏病と呼ばれる不随意運動で、神経症状の一つです。
• 「何だか目がうつろ」「呼びかけに反応しない」
◦ 特に高齢者のHHSでは、意識障害が前面に出ることが多く、家族に連れてこられるパターンもあります。
DKAとHHS
原因
高血糖緊急症の誘因:5つの「I」
1. Infection(感染症)
• 最も一般的な誘因です(DKAの20-40%、HHSの32-60%)。
• 特に肺炎と尿路感染症が多く、敗血症に至ることもあります。
2. Insulin(インスリンの中断・不足)
• 治療の中断や不適切な使用です。
• 「シックデイ」の誤解: 胃腸炎などで食事がとれないときに、「食べていないからインスリンは要らない」と誤って中止してしまうケースが含まれます。
• 若い1型糖尿病患者での意図的な中断(体重増加への恐怖や摂食障害など)や、インスリンポンプの故障も原因となります。
3. Initial presentation(初発・新規発症)
• 新規発症の糖尿病です。糖尿病と診断されていない人が、最初の症状(DKAなど)として搬送されるケースです。
• 特に1型糖尿病の約20〜25%はDKAで発症します。
4. Ischemia / Infarction(虚血・梗塞・重篤な疾患)
• 身体への強いストレスとなる急性疾患です。
• 心筋梗塞、脳卒中(脳血管障害)、急性膵炎、肺塞栓症などが挙げられます。
5. Iatrogenic / Ingestion(医原性・薬剤・摂取)
• 血糖値を上げる薬剤や物質の影響です。
• 薬剤: ステロイド、SGLT2阻害薬(正常血糖DKAの原因になる)、チアジド系利尿薬、抗精神病薬(クロザピンなど)。
• 物質: コカインの使用やアルコール乱用も関連しています。
鑑別
糖尿病ケトアシドーシス(DKA)と高浸透圧高血糖状態(HHS)は、ともに糖尿病の急性合併症(高血糖緊急症)ですが、病態や臨床像、検査所見に明確な違いがあり、これらを組み合わせて鑑別します。
一般的に DKA は症状の進行が速くおおむね 1 日で進行します。一方HHSは数日かけ
て症状の進行がみられることが多いです。
米国糖尿病学会(ADA)の診断基準に基づくと、以下の数値が鑑別の目安となります。
| 検査項目 | DKA (糖尿病ケトアシドーシス) | HHS (高浸透圧高血糖状態) |
|---|---|---|
| 血糖値 | > 250 mg/dL | > 600 mg/dL(著明な高血糖) |
| 動脈血 pH | ≦ 7.30 (アシドーシスあり) | > 7.30(正常範囲が多い) |
| 血清重炭酸イオン (HCO3-) | ≦ 18 mEq/L(低値) | > 18 mEq/L |
| 尿中・血中ケトン体 | 陽性 | 陰性 〜 弱陽性 |
| 有効血清浸透圧 | さまざま | > 320 mOsm/kg (著明な高浸透圧) |
| アニオンギャップ | > 10 〜 12(開大) | さまざま(通常は正常) |
| 意識障害 | 軽度〜昏睡まで様々 | 昏迷・昏睡が多い |
• DKAの特徴: インスリンの絶対的欠乏により、脂肪分解が進んでケトン体が産生され、代謝性アシドーシス(血液が酸性になる)を呈するのが最大の特徴です。
• HHSの特徴: インスリン作用不足はあるもののケトン体産生を抑制する程度には保たれているためアシドーシスにはなりにくく、極度の高血糖による脱水と高浸透圧が病態の中心です
治療
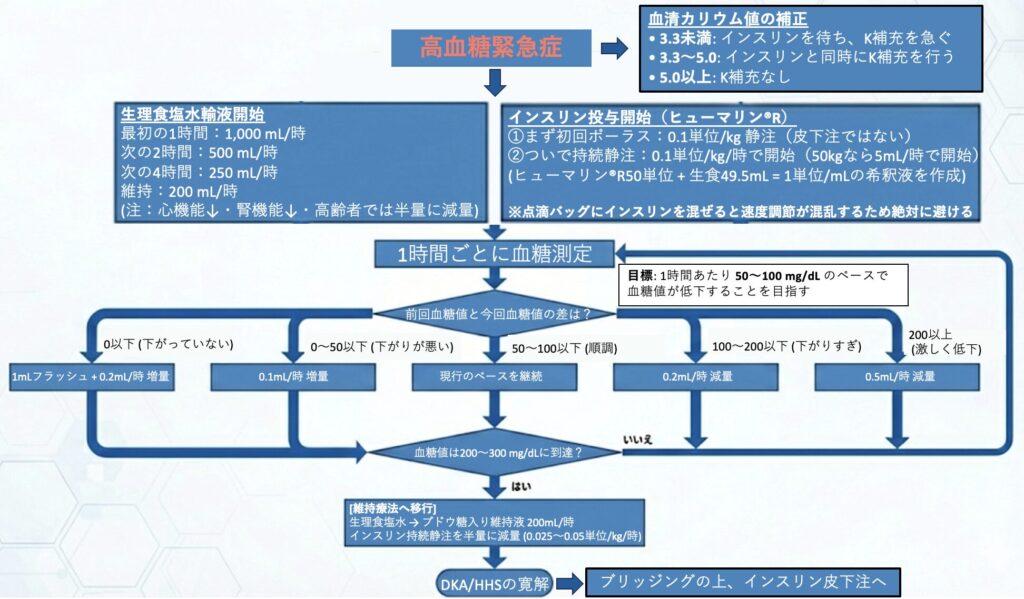
DKAおよびHHS治療における具体的な投与量と手順をまとめます。
治療は「生理食塩水の大量輸液」と「インスリン持続静注」と「血清カリウム管理」の3本柱で行います。
1. 生理食塩水大量輸液(脱水の補正)
まずは脱水の補正を優先します。心機能、腎機能、高齢者などで問題がある場合は、以下の量を半量にするなどベースダウンを検討します。
• 使用する輸液: 生理食塩水
• 投与スケジュール:
1. 最初の1時間: 1,000 mL/時
2. 次の2時間: 500 mL/時
3. その後の4時間: 250 mL/時
4. 維持: 200 mL/時
• 輸液の切り替えタイミング:
◦ 血糖値が 200〜300 mg/dL まで低下したら、生理食塩水から ブドウ糖入りの維持輸液 200 mL/時 に変更し、低血糖を予防します。
なお、「2.次の2時間」以降はVolumeをみつつ速度を調整します。私は、Volumeの評価はIVC径の経時的変化をみて判断しています(賛否両論あるかと思います)。尿量をVolumeの評価に用いるか、についてですが、高血糖ですと浸透圧利尿が起こるためvolume評価の指標にはあまりならないかなと個人的には考えています。
2. インスリン静注(血糖コントロール)
インスリンは「1時間ごとの血糖変動(差)」を見て、流量を細かく調整します。
準備(インスリン溶液の作成)
• 速効型インスリン(ヒューマリン®Rなど)50単位(0.5 mL) + 生理食塩水 49.5 mL
• 合計 50 mL とすることで、濃度を 1 単位/mL に調整します。
開始手順
1. 初回ボーラス投与: 速効型インスリン 0.1 単位/kg を静注します。
◦ (例:体重50kgなら 5単位を静注) (追記:専門医の先生に聞いたところボーラス投与は不要とのことです。)
2. 持続静注開始: 直後にシリンジポンプで 0.1 単位/kg/時 で開始します。
◦ (例:体重50kgなら 5 mL/時 = 5単位/時)
調整プロトコル(1時間ごとのチェック)
1時間ごとに血糖値を測定し、「前回(1時間前)の血糖値 - 今回の血糖値」 を計算して、その差に応じて流量を以下の通り変更します。
| 血糖値の差(前回-今回) | 判定 | 対応(流量調整) |
|---|---|---|
| 0 以下 | 下がっていない | 1 mL フラッシュ(早送り)して、0.2 mL/時 増量 |
| 0 超 〜 50 以下 | 下がりが悪い | 0.1 mL/時 増量 |
| 50 超 〜 100 以下 | 順調 | そのまま現行ペースで続行 |
| 100 超 〜 200 以下 | 下がりすぎ | 0.2 mL/時 減量 |
| 200 超 | 激しく低下 | 0.5 mL/時 減量 |
• 目標: 1時間あたり 50〜100 mg/dL のペースで血糖値が低下することを目指します。
減量のタイミング
• 血糖値が 250〜300 mg/dL になれば、インスリン持続静注量を 半量(もしくは 0.025〜0.05 単位/kg/時)に減量します。
• このタイミングで、前述の「ブドウ糖入りの維持輸液」への変更を同時に行います
3. 血清カリウムの管理
高血糖緊急症(DKAおよびHHS)におけるカリウムの管理は、インスリン投与と同じくらい重要です。インスリン治療を行うと血中のカリウムが細胞内に移動し、急激に数値が低下するため、必ずインスリン開始前にK値を確認し、値に応じた補充を行います。
(※なおインスリンの投与に伴い,低リン血症も生じ得るので注意が必要です)
1. カリウム値による対応フロー
血清カリウム値によって、インスリンを開始できるかどうか、およびカリウム補充の速度が異なります。
① K < 3.3 mEq/L の場合(低カリウム)
この状態でインスリンを入れると致命的な不整脈を招く危険があるため、インスリン投与は待機し、まずカリウムの補充を優先します。
• 処方: 塩化カリウム(20 mEq)+ 生理食塩水 500 mL
• 速度: 1時間で点滴
• 注意: K値が上昇してからインスリンを開始します。
② K = 3.3 〜 5.0 mEq/L の場合(正常〜低値傾向)
体内の総カリウム量は不足していることが多いため、インスリン投与と並行してカリウムを補充します。
• 処方: 塩化カリウム(20 mEq)+ 生理食塩水 500 mL
• 速度: 2時間で点滴
• 輸液調整の工夫:
◦ 脱水補正のためにトータルの輸液速度を「500 mL/時」確保したい場合は、上記のカリウム入り輸液(250 mL/時相当)とは別に、「Kなしの生理食塩水 500 mLを2時間で点滴(=250 mL/時)」するラインを同時に走らせる方法があります。
③ K > 5.0 mEq/L の場合(高カリウム)
現時点での補充は不要です。ただし、治療経過で低下してくる可能性があるため、定期的なチェックは欠かせません。
2. なぜカリウム補充が必要なのか
以下の理由からカリウム管理が重要視されています。
• 検査上のK値が正常に見えても、アシドーシスの影響で細胞内から血管内にKが移動しているだけで、体内の総カリウム量は絶対的に不足しています(DKAで3-5 mEq/kg、HHSで4-6 mEq/kgの喪失)。
• インスリンによる低下: 治療でインスリンが入ると、Kが細胞内に戻っていくため、血清K値は急激に低下します。補充を行わないと重篤な低カリウム血症に陥るリスクがあります。
カリウム補正まとめ
• 原則: インスリン開始前にK値をチェックする。
• 3.3未満: インスリンを待ち、K補充を急ぐ。
• 3.3〜5.0: インスリンと同時にK補充を行う。
• 5.0以上: 補充なしで開始し、経過を追う。
速効型インスリン持続静注から皮下注射へ切り替えるタイミング
糖尿病性ケトアシドーシス(DKA)の切り替えタイミング
DKAは以下の状態になれば回復したと判断し、皮下インスリン注射へ移行します。
「食事摂取が可能である」かつ「血糖値の基準に加え、その他2項目以上」を満たす必要があります。
■食事摂取が可能
■血糖値<200 mg/dL
■以下のうち2項目以上を満たす
- 静脈血pH>7.3
- 血清重炭酸イオン濃度 (HCO3-)≧15 mEq/L
- アニオンギャップ (AG)≦12 mEq/L
- ※尿中ケトン体は、DKA改善後も陽性が続くため指標とならない。
具体的な対応: アシドーシスが改善し、食事が摂れるようになった段階で、速効型インスリン(または超速効型)の皮下注射と、持効型インスリン(基礎インスリン)の併用(強化インスリン療法)へ切り替えます。 ⇢強化インスリン療法についての記事はこちら
※なお、インスリン静注を中止する際は、血中インスリン濃度が切れないように、皮下注射を行ってから一定時間(例:2-4時間)併用した後にインスリン静注を止めることが重要です(ブリッジングといいます。インスリン静注の半減期は10分程度と短い!)。
高浸透圧高血糖状態(HHS)の切り替えタイミング
HHSの病態は著しい高血糖と「高度な脱水」であるため、脱水の補正が治療の中心となります。
HHSは以下の状態になれば回復したと判断し、皮下インスリン注射へ移行します。
• 脱水状態からの回復: 十分な輸液により循環動態が安定すること。
• 意識状態の改善: 意識障害が改善すること。
• 食事摂取可能(HHSは高齢者に多く、嚥下機能に要注意です)。
まとめ
臨床的な寛解の目安は以下の通りです。
| 病態 | 回復・切り替えの目安(要点) |
|---|---|
| DKA | アシドーシスの消失 かつ 食事が食べられる |
| HHS | 脱水の改善(循環安定) かつ 意識の回復 かつ 食事が食べられる |
切り替え方法
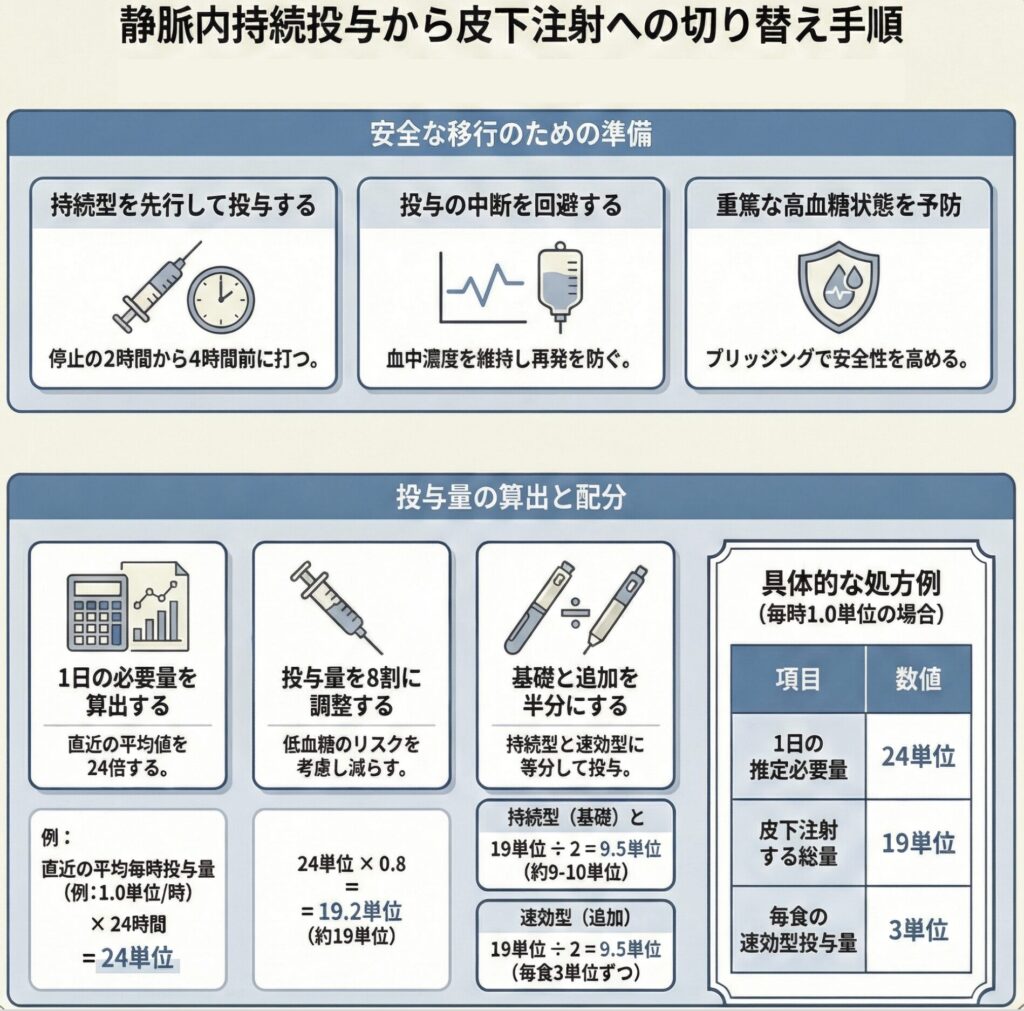
1. 1日必要量の推測
切り替え前 6時間の平均インスリン持続投与流量(単位/時) を24倍して、1日のインスリン必要量を算出します。
◦ 計算式:平均流量(単位/時) × 24
2. 皮下注総量の決定(80%ルール)
推測した1日必要量の 80% を、実際に皮下注するインスリン総量とします。
◦ 計算式:推測した1日量 × 0.8
3. 持効型と速効型インスリンの投与量を決める
皮下注総量の 半量を持効型インスリン(基礎分泌用)、残りを速効型インスリン(追加分泌用)に分けます。
4. 投与タイミング
◦ 持効型: 1日1回(または指示通り)投与。
◦ 速効型: 上記で算出した量を、食事に合わせて 1日3回に分割投与 します。
◦ ※食事量に応じて増減し、絶食時は打ちません。食事量が不安定な場合は「食後打ち」にして量で調整します。
実際のケースで考えてみよう
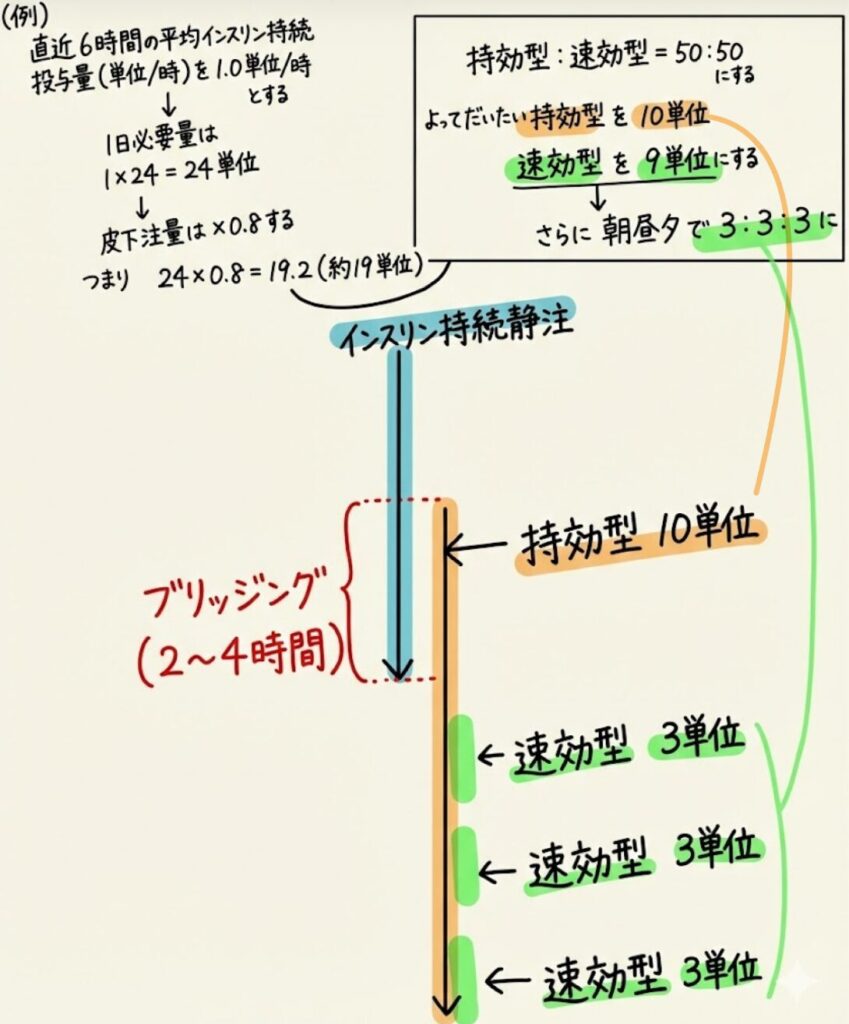
DKA治療後、状態が安定し食事が摂れるようになった。 直近6時間のインスリン持続点滴の平均流量は 1.0 単位/時 であった。
【計算ステップ】
1. 1日必要量の推測: 1.0 単位/時 × 24時間 = 24 単位
2. 皮下注総量の決定(×0.8): 24 単位 × 0.8 = 19.2 単位(約19単位とします)
3. 配分(持効型と速効型を半々にする):
◦ 持効型インスリン: 19単位の半分 ≒ 10 単位 を1日1回。
◦ 速効型インスリン: 残りの 9〜10 単位 を3回の食事に分ける。
4. 実際の指示例:
◦ 持効型(グラルギンなど):10 単位 寝る前
◦ 速効型(リスプロなど):毎食直前 3 単位(3単位×3回=9単位)
このように、点滴で必要だった量よりも少し少なめ(80%)から開始することで、切り替え直後の低血糖リスクを回避します。
参考文献
- UpToDate – Diabetic ketoacidosis and hyperosmolar hyperglycemic state in adults_ Clinical features, evaluation, and diagnosis (2026/02/05閲覧)




コメント