夜間の当直中、呼吸苦を訴える患者さんが搬送されてきたとき、皆さんは自信を持って初期対応ができていますか?
急性心不全は時間との勝負です。「最初の10分」で行うべきトリアージから、「次の60分」で行う病態評価と治療戦略まで、その判断スピードが患者さんの予後を大きく左右します。
初期対応の方法、そして病態生理を考えつつ治療薬を選択するために大切な「Nohria-Stevenson分類」についてもまとめました。
急性心不全の初期対応
- 心不全ガイドライン2025では、時間軸を意識した「トリアージ(最初の10分)」から「病態評価と治療(次の60分)」への流れが推奨されています。
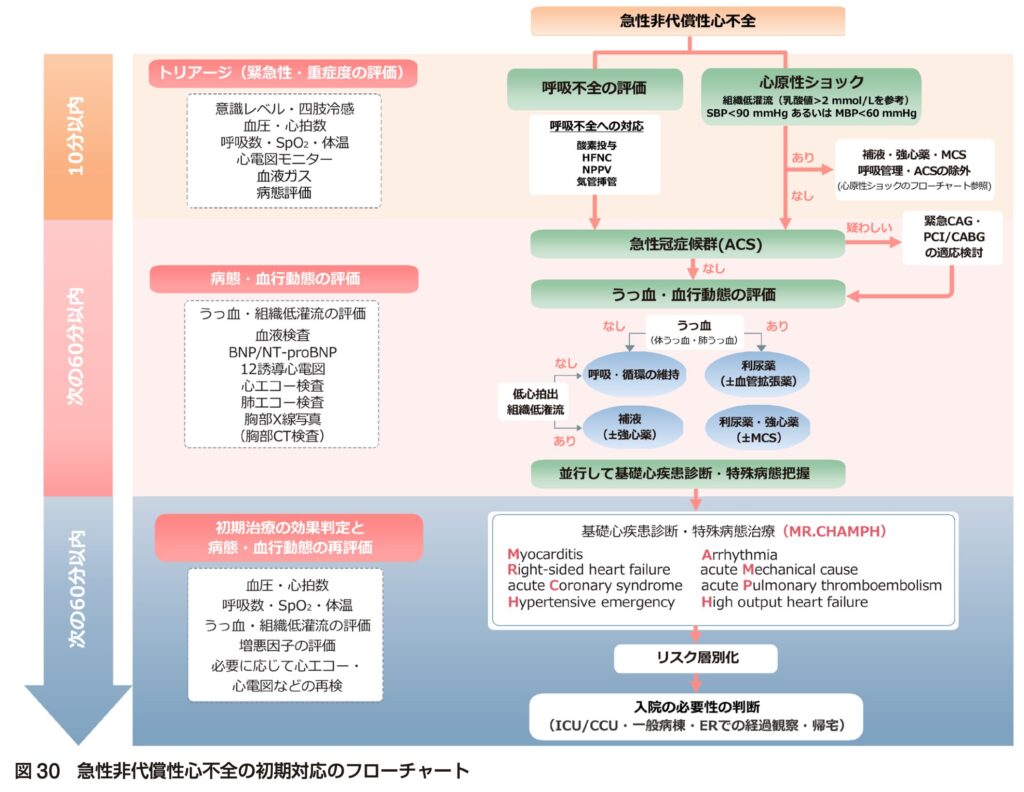
1. トリアージ:緊急度・重症度の評価(最初の10分以内)
- 救急搬送直後などは、まず「生命の危機」に直結する病態の有無を判断し、安定化を図ります。
呼吸不全への対応
- SpO2 < 90% または PaO2 < 60 mmHg で酸素投与を速やかに行います。
- 呼吸困難が改善しない場合(呼吸数>25回/分など)は、速やかにNPPV(非侵襲的陽圧換気)を導入します。⇢NPPVについてはこちらにまとめました。
- 改善がなければ気管挿管を検討します。⇢気管挿管についてはこちらの記事にまとめました。
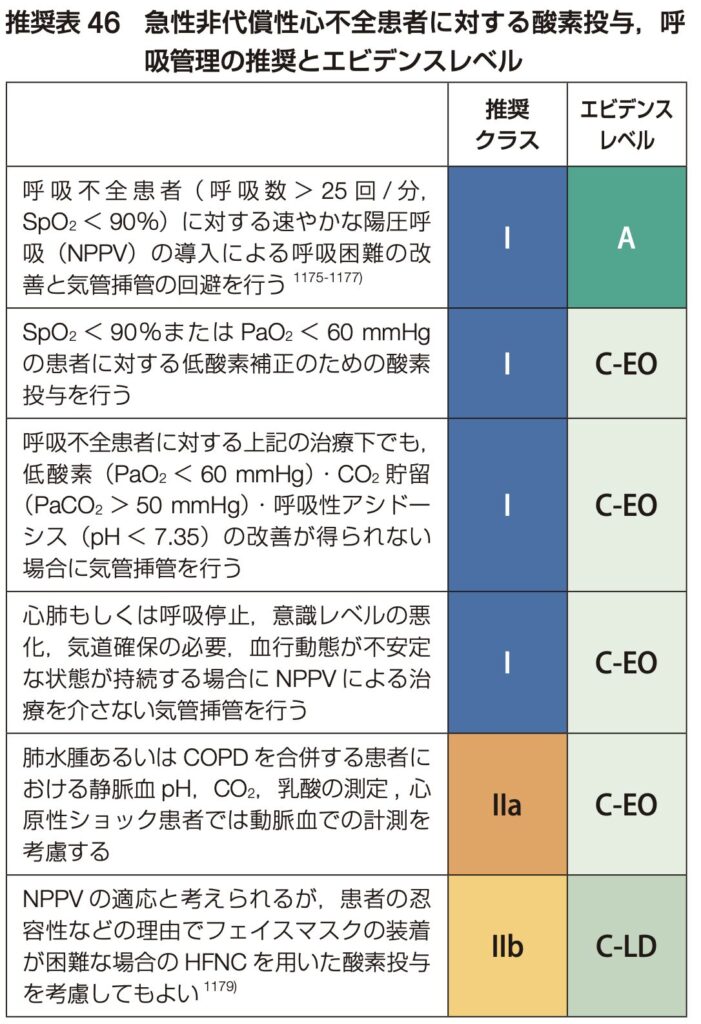
心原性ショックの評価
- 収縮期血圧 < 90 mmHg、四肢冷感、意識障害、乳酸値上昇(>2 mmol/L)などを確認します。
- ショックがある場合は、循環器内科医に相談しつつ、強心薬(ドブタミンなど)や昇圧薬(ノルアドレナリン)の使用、および機械的補助循環(MCS: IABP, Impella, PCPS/ECMO)の適応を検討します
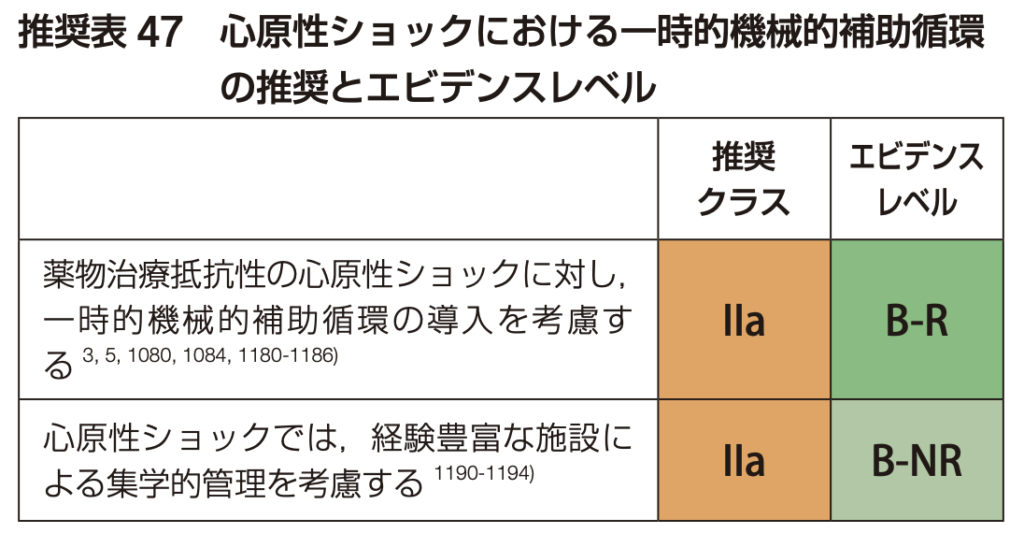
急性冠症候群(ACS)の除外
以下の検査を行い、ACSが疑われる場合は、緊急カテーテル検査・再灌流療法へ進みます。
- 12誘導心電図: 急性非代償性心不全の初期評価において速やかに実施し、ACS(ST変化など)や不整脈の有無を確認します。
- 心筋トロポニン: 心筋障害のバイオマーカーとして測定されます。ACS診断の鍵となるほか、ACSがない場合でもトロポニンの持続的な高値は「ステージB(前心不全)」の定義に含まれるなど、リスク評価にも用いられます。
- 心エコー検査: 壁運動異常の有無を確認することで、虚血性心疾患の可能性を評価します。
- 冠動脈CT: 「除外」において特に有用とされています。ガイドラインでは、虚血性心疾患の検査前確率が「低~中等度」の心不全患者において、冠動脈疾患を除外するために冠動脈CTを考慮することが推奨されています(推奨クラスIIa)。また、呼吸困難の鑑別として行われる胸部CTでも、ACSの評価が含まれる場合があります。ただし、造影する必要があるので初期対応の場面で行うことはないです。
2. 病態・血行動態の評価と初期治療(次の60分以内)
- 致死的状況を回避したら、身体所見(Nohria-Stevenson分類の視点)を用いて血行動態を評価し、治療薬を選択します。Nohria-Stevenson分類についてはのちほど解説します。
- A. うっ血の評価(Wet vs Dry)
- 所見: 頸静脈怒張、ラ音、浮腫、BNP上昇など。
- B. 低灌流の評価(Cold vs Warm)
- 所見: 四肢冷感、脈圧狭小、意識レベル低下、腎機能悪化など。
対応
- Wetの場合
- ループ利尿薬の静注が第一選択です。
- 投与量: 初回 20〜40 mg、または内服中の患者は内服量の1〜2倍量を静注します。
- 効果判定: 投与1〜2時間後に尿量(>100 mL/時など)を確認し、反応不良なら倍量投与や併用(サイアザイド系、トルバプタンなど)へ強化します。
- 血管拡張薬: 血圧が保たれている(収縮期血圧 > 110 mmHgなど)、特にクリニカルシナリオ1(高血圧性急性心不全)のような病態では、硝酸薬(ニトログリセリン、硝酸イソソルビド)の併用を考慮します。
- ループ利尿薬の静注が第一選択です。
- Coldの場合
- 強心薬(ドブタミン、PDEIII阻害薬): 低心拍出による臓器低灌流がある場合に考慮します(推奨クラスIIa)。ただし、ルーチンでの使用は予後を悪化させる可能性があるため避けます。
- 昇圧薬(ノルアドレナリン): ショック(著明な低血圧)がある場合に使用します。
- しかし、低灌流所見がある時点で循環器内科医にcallし判断を仰ぐべきと私は思います。
3. 原因・増悪因子の検索(MR.CHAMPH)
- 初期治療と並行して、心不全を増悪させた原因を検索し、特異的な治療を行います。覚え方として「MR.CHAMPH(ミスターチャンプ)」などが知られています。
- M: Myocarditis (心筋炎)
- R: Right-sided heart failure (右心不全)
- C: acute Coronary syndrome (急性冠症候群)
- H: Hypertensive emergency (高血圧緊急症)
- A: Arrhythmia (不整脈)
- M: acute Mechanical cause (機械的合併症:弁膜症、腱索断裂など)
- P: acute Pulmonary thromboembolism (急性肺血栓塞栓症)
- H: High output heart failure (高拍出性心不全:貧血、甲状腺機能亢進症など)
4. まとめ:初期対応のフロー
- ショック・呼吸不全はないか? → あればNPPV、強心薬/昇圧薬、MCS。
- うっ血(Wet)はあるか? → あれば利尿薬静注(早期に効果判定)。
- 血圧は高いか? → 高ければ血管拡張薬併用。
- 原因は何か? → ACSや不整脈などを除外・治療。
- このプロセスを、最初の数時間以内に迅速に回していくことが求められます。
心エコーでの評価項目
- 救急外来でどこまでエコーをすべきかは様々な意見があるかと思います。私自身がチェックしている項目を下記図にまとめました(賛否両論あるかと思います。間違いや「もっとここをみるべきだ!」などご意見があれば、コメントで教えていただけますと幸甚です)。
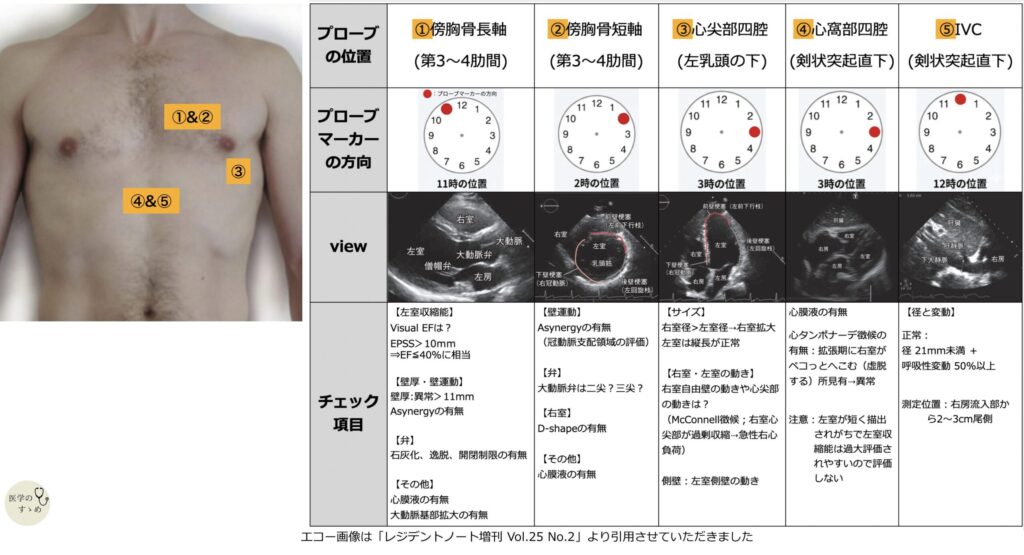
Nohria-Stevenson分類を用いた治療薬の選び方
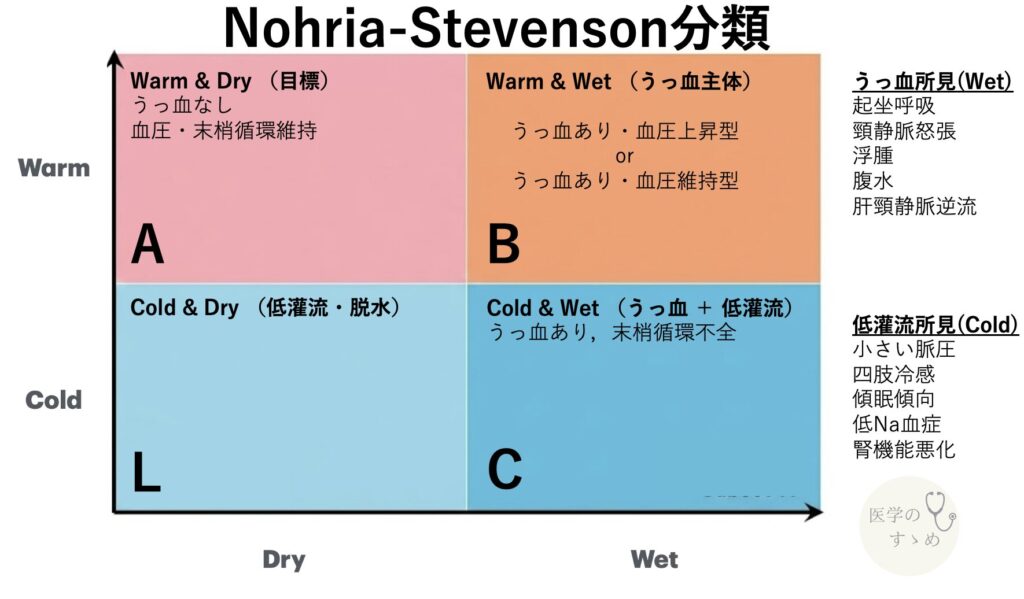
心不全治療で「なぜ利尿薬?血管拡張薬?」と迷うことはありませんか?その答えはNohria-Stevenson分類にあります。Nohria-Stevenson分類とはまずなんなのか、説明していきます。
Nohria-Stevenson分類は、急性心不全患者の初期評価において、スワンガンツカテーテルなどの侵襲的な検査を用いず、身体所見だけで血行動態を推定し、重症度や治療方針を決定するための分類法です。
この分類では、「うっ血の有無(Wet vs Dry)」と「末梢組織灌流の良否(Warm vs Cold)」の2つの軸を組み合わせて、患者を4つのプロファイルに分類します。
評価の軸
縦軸:うっ血所見(Wet / Dry) 肺や全身に水が溜まっているかを評価します。
- Wet(うっ血あり): 左心不全徴候: 起坐呼吸、夜間発作性呼吸困難、聴診での湿性ラ音(水泡音)、III音・IV音など ・ 右心不全徴候: 頸静脈怒張、下腿浮腫、腹水、肝腫大、肝頸静脈逆流など
- Dry(うっ血なし): 上記の所見がない場合
横軸:組織低灌流所見(Warm / Cold) 心臓が全身に十分な血液を送り出せているかを評価します。
- Cold(低灌流あり): 四肢冷感: 手足が冷たい ・ 低い脈圧: (収縮期血圧-拡張期血圧)が小さい ・ 意識レベルの低下 ・ 乏尿、腎機能の悪化
- Warm(灌流良好): 上記の所見がなく、手足が温かい場合
4つの臨床プロファイルと特徴
これらを組み合わせて、以下の4つに分類します。
- Profile A (Dry & Warm):うっ血なし、灌流良好
- 安定しており、最も軽症な状態です。
- Profile B (Wet & Warm):うっ血あり、灌流良好
- 急性心不全で最も頻度が高いタイプです。
- 血圧は保たれていることが多く、治療は利尿薬や血管拡張薬、NPPVによるうっ血の解除が中心となります。
- Profile L (Dry & Cold):うっ血なし、低灌流あり
- 頻度は少ないですが、脱水や循環血液量減少などが考えられます。
- 心不全の治療中に利尿薬を効かせすぎてこの状態になることもあります。
- Profile C (Wet & Cold):うっ血あり、低灌流あり
- 心原性ショック(またはその前段階)に相当する最重症タイプです。 ⇢循環器内科医callの必要あり
- 心ポンプ機能が著しく低下しており、単なる利尿薬投与だけでは血圧が維持できずショックが悪化するリスクがあります。
- 強心薬や昇圧薬、場合によってIABP、PCPSなどの導入を検討する必要があります
利尿薬・血管拡張薬・血管拡張薬はNohria-Stevenson分類上の点をどう移動させるか
利尿薬
利尿薬はNohria-Stevenson分類の表において「右(Wet)から左(Dry)」へ移動させる力(前負荷を下げ、うっ血をとる力)が主体です。
血管拡張薬
血管拡張薬が力は、主に以下の2つの合成になります。
- 右から左へ(静脈拡張): 血液を末梢の静脈にプールさせる(血管容量を広げる)ことで、心臓に帰ってくる血液量(前負荷)を減らし、肺うっ血を改善します。これは利尿薬と同じ「右から左」へのベクトルですが、利尿薬が「水を体外に出す」のに対し、血管拡張薬は体内で水を移動させる(再分布)点が異なります。
- 下から上へ(動脈拡張): 末梢血管の抵抗(後負荷)を下げることで、心臓が血液を送り出しやすくします。これにより、心拍出量が増加し、「Cold」から「Warm」方向へ持ち上げる力が働きます。
つまり、血管拡張薬はNohria-Stevenson分類の表でいうと「右から左へ移動させつつ、少し上へ持ち上げる(左斜め上への)力」があると言えます。
強心薬
「下から上へ」移動させます。
Nohria-Stevenson分類の縦軸は「組織灌流(CI:心係数)」を表しています。強心薬は心筋の収縮力を増強させ、心拍出量(CO/CI)を増加させます。これにより、表の下側にある「Cold(低灌流・ショック)」の状態から、上側の「Warm(灌流良好)」の状態へ患者を持ち上げることができます。
症例1
では例をみてみましょう。下図の「症例1」を御覧ください。血圧が上昇していて、ラ音を聴取する・・・つまり、Warm&Wetのパターン(CSでいうとCS1)ですね。血液の異常分布のパターンですので利尿薬だけですとWarm&Dry(目標)に到達できません。そこで血管拡張薬も併用します。
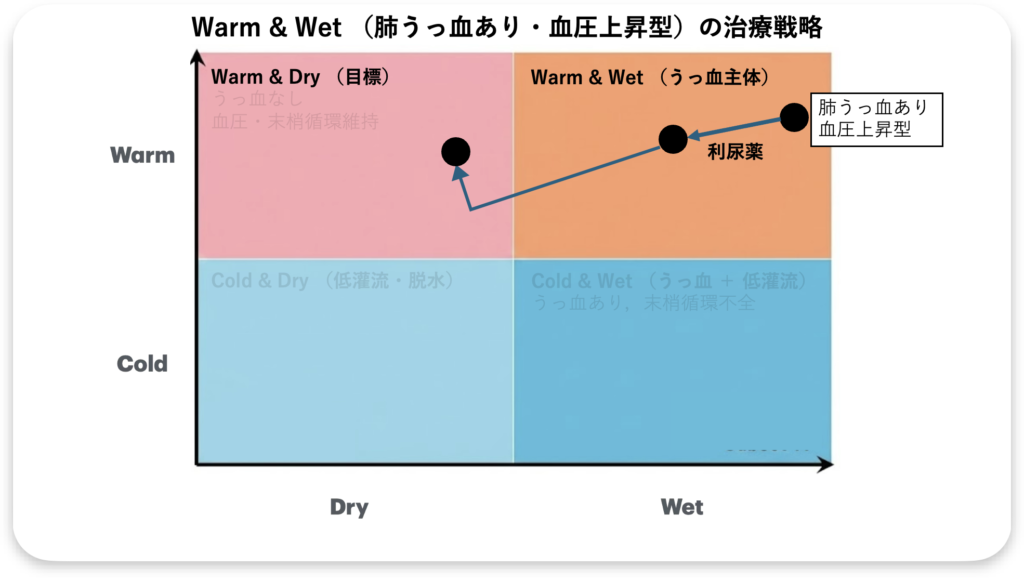
症例2
つぎの例をみてみましょう。下図の「症例2」を御覧ください。血圧は低下も上昇もしていないが、全身に浮腫がありそう・・・つまり、Warm&Wetのパターン(CSでいうとCS2)ですね。ここでは体うっ血がメインなので利尿薬で十分そうです。血管拡張薬を使用すると血圧が下がりすぎる可能性があります。私はこのパターンでは利尿薬のみに留めています。
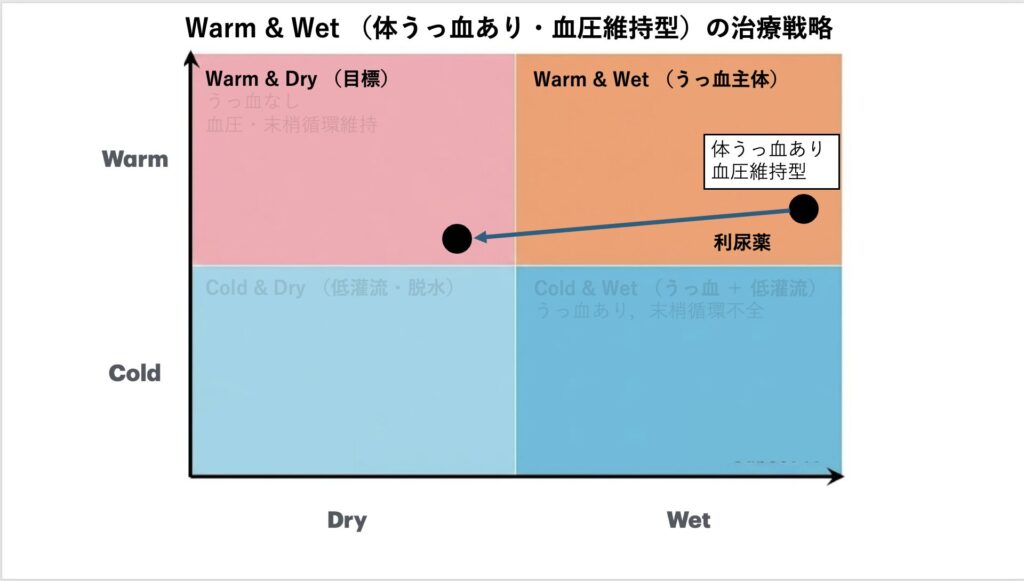
症例3
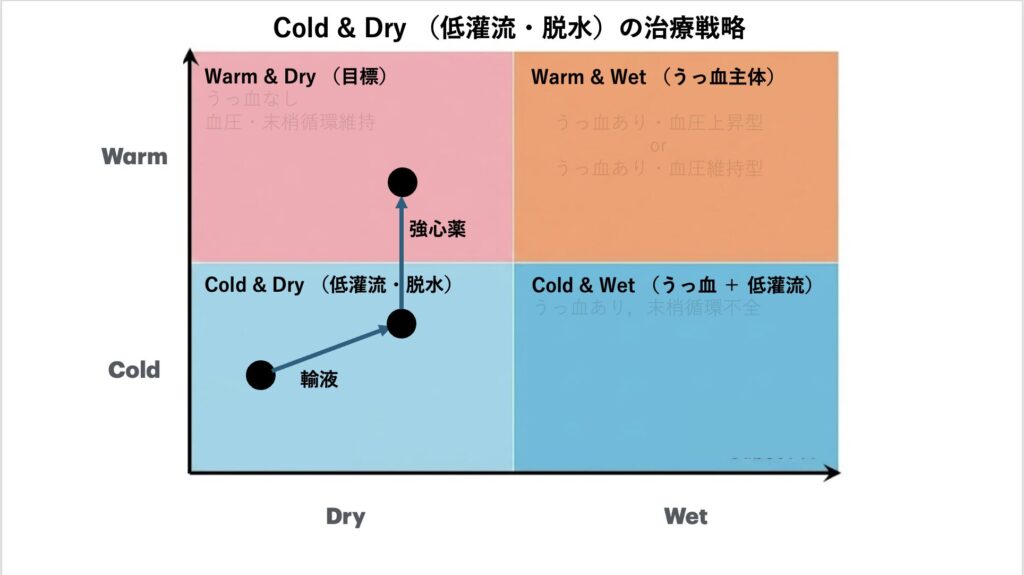
症例3をみてみましょう。末梢が冷たく血圧が低い。ラ音もなく浮腫もない。「Cold&Dry」のパターンです。Cold & Dry(Profile L)は、組織低灌流(Cold)があるものの、うっ血(Wet)がない状態です。 これは、心機能が低下していることに加え、「循環血液量が不足している(脱水)」や「前負荷が足りていない」可能性が高いことを示唆します。
心臓の中に血液が十分に入っていない状態(低前負荷)で強心薬を使って無理やり収縮させても、送り出す血液がないため心拍出量は増えず、心筋の酸素消費量を増やすだけで終わってしまいます(「空打ち」に近い状態)。
フランク・スターリングの法則を思い出してみましょう。心臓は適度な張り(前負荷)があって初めて強く収縮できます。まずは輸液で心室を満たし、ポンプとしての効率を発揮できる環境を整える必要があります。
2025年版の心不全診療ガイドラインにおいても、この病態に対する初期対応として補液が明記されています。
• 初期対応フローチャート:で「低心拍出・組織低灌流あり(Cold)」かつ「うっ血なし(Dry)」の分岐において、治療内容は「補液(± 強心薬)」と記載されています。「体液貯留が認められない患者に対して、生理食塩水あるいはリンゲル液の急速輸液(15~30分で200mL以上)を考慮する(推奨クラスIIa)」とされています。
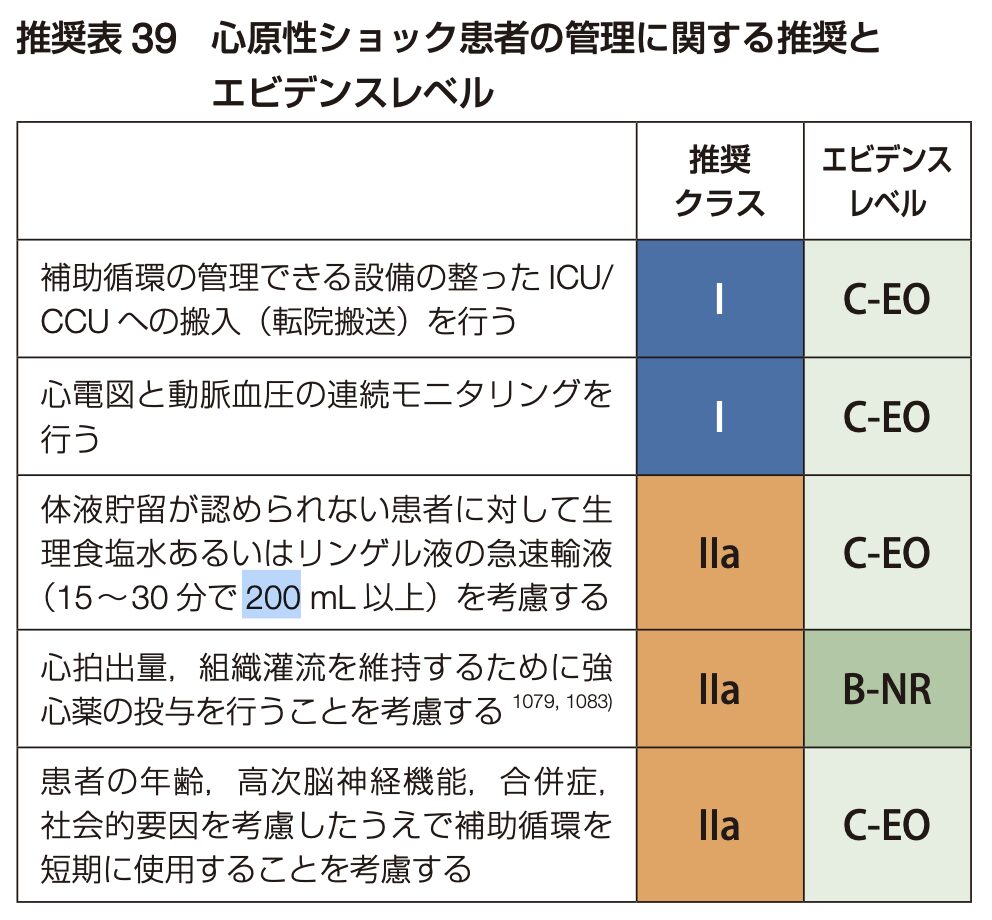
よって、まず細胞外液などを慎重に投与し、前負荷を増やします。輸液で前負荷を確保した上で強心薬の併用を行います。
肺うっ血だろうが、体うっ血だろうが利尿薬を投与すべきなのか?肺うっ血だけでも投与すべきか?
うっ血があれば利尿薬は基本
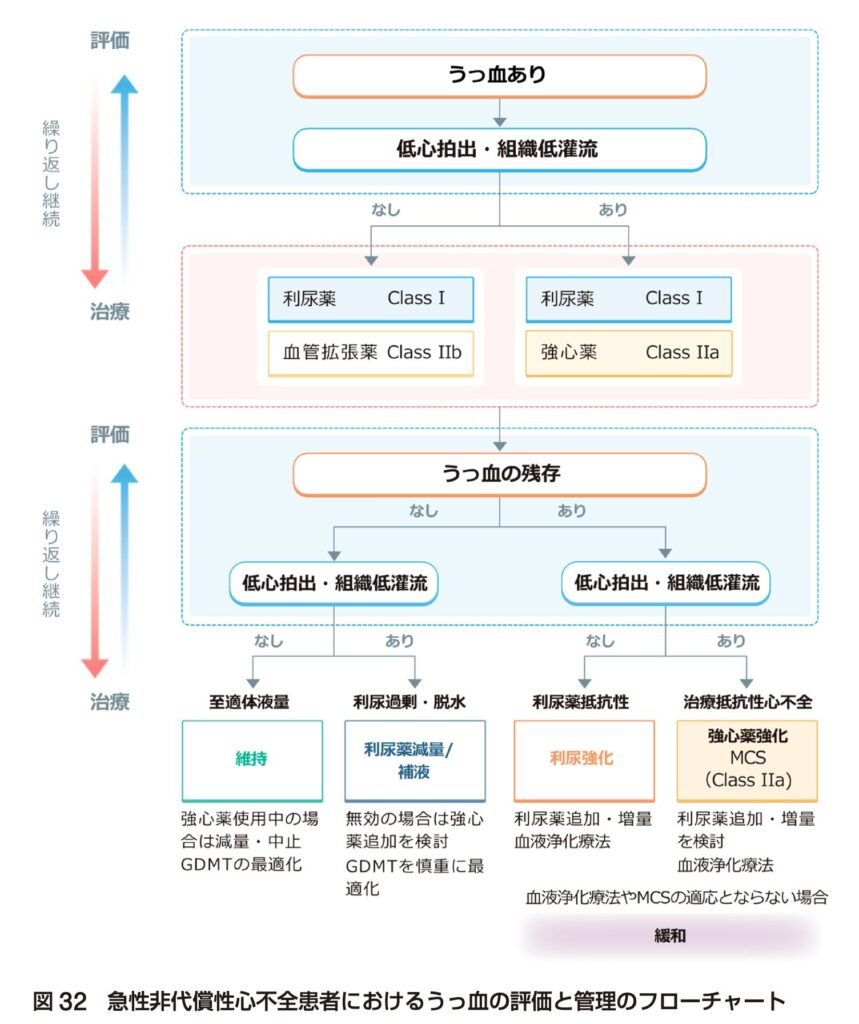
心不全ガイドライン2025を読むとうっ血(体うっ血・肺うっ血)あり⇢利尿薬±血管拡張薬と記載があります。また、「肺うっ血による呼吸困難を解消することは,急性非代償性心不全初期治療の重要な目的である.うっ血治療の中心は利尿薬であり,体液貯留の所見が確認されれば速やかにループ利尿薬を静脈内投与する.」とも記載されています。つまり、新しいガイドラインではうっ血がある場合は、体うっ血だろうが、肺うっ血だろうが利尿薬を投与すべきと解釈できます。
• 体うっ血(浮腫、頸静脈怒張など): 体液量の絶対的な増加(Volume Overload)を示唆するため、利尿薬による除水が必須です。
• 肺うっ血(呼吸困難、ラ音など): 左室充満圧の上昇を示しており、利尿薬で前負荷を軽減することが有効です。
私自身、肺うっ血か体うっ血かに関わらず、原則としてループ利尿薬の静脈投与はまずは行うべきと考えています。体うっ血(浮腫、頸静脈怒張など)であれば体液量の絶対的な増加(Volume Overload)を示唆するため、利尿薬による除水が有効となります。肺うっ血(呼吸困難、ラ音など)であれば左室充満圧の上昇を示しており、利尿薬で前負荷を軽減することが有効です。
ただし、肺うっ血単独の場合や血圧の状況によって、利尿薬よりも優先される治療がある場合もあります。
「肺うっ血だけ」の場合の注意点
「肺うっ血はあるが、体うっ血はない」というケース(いわゆるクリニカルシナリオ1など)では、対応が少し異なります。病態としては、体全体の水分量はそれほど増えておらず、血管収縮によって血液が肺に移動している「体液再分布」が主体です。この場合、利尿薬も使いますが、血管拡張薬(硝酸薬など)で血管を広げて血液を末梢へ逃がす治療が併用することが多いです(私見)。
利尿薬を投与すべきでない(注意すべき)例外
うっ血があっても、以下の状況では利尿薬の投与を控える、あるいは極めて慎重に行う必要があります。
• 低心拍出・ショック(Cold)の状態: 血圧が低い(収縮期血圧 < 90 mmHgなど)、四肢冷感がある場合は、利尿薬で前負荷を下げるとさらに血圧が下がり、ショックが悪化する危険があります。 この場合は、まず強心薬などで循環を安定させてから(Warmにしてから)、慎重に利尿薬を使用します。
血管拡張薬の使いどころ
血管拡張薬が著効する患者像
血管拡張薬が最も効果を発揮するのは、「血圧が高く、急激に発症した肺うっ血」のケースです(クリニカルシナリオでいうと1のケースです)。
収縮期血圧 > 140 mmHg の高血圧性急性心不全。
◦ 急激な呼吸困難で発症し、全身のむくみ(体液貯留)よりも、肺水腫が主体です。
• Nohria-Stevenson分類:
◦ Wet & Warm(うっ血あり、末梢循環良好)で、特に血圧が高いケース。
なぜ血管拡張薬を使うのか?
この病態の本質は、体全体の水分量が増えすぎているわけではなく、「血液の分布異常(再分布)」だからです。
• 後負荷の軽減(動脈拡張): 血圧(後負荷)が高いと、心臓が血液を全身に送り出せず、手前にある肺に血液がバックしてしまいます。血管を広げて血圧を下げることで、心臓が楽に拍出できるようになります。
• 静脈還流の減少(静脈拡張): 静脈を広げることで、血液を体の末梢(手足などの静脈)にプールさせます。これにより、肺に集中していた血液を散らし、肺うっ血を速やかに改善します。
・利尿薬との違い: 利尿薬は尿として水を出すのに時間がかかりますが、血管拡張薬は即効性があり、この病態(CS1)では利尿薬よりも優先、あるいは併用されます。
主な薬剤と使い分け
主に以下の3剤が使用されますが、救急では硝酸薬(ニトログリセリン)が第一選択となることがほとんどです
| 薬剤名 | 具体的な使用量・投与法 | 特徴・使い所 | 注意点 |
|---|---|---|---|
| 硝酸薬 (ニトログリセリン:ミリスロール®、ミオコール®等) | 【開始量】 0.05~0.1 γ (μg/kg/min) で開始。 (医師によっては「2mL/hrで開始」としているが、これだと過降圧になりやすいように感じます) 【調整】 5~10分ごとに 0.1~0.2 γ ずつ増量。収縮期血圧 140mmHg以下、または初期値から20-25%低下を目標とする | 【第一選択】 動脈・静脈の両方を拡張させ、特に肺うっ血の軽減に優れる。即効性があるため調節しやすい。 まずはミオコール舌下スプレー (1puff0.3mgを1~2回噴霧) でもOK⇢ルート確保しやすくもなります。 | 耐性(48時間程度で効果減弱)に注意。 右室梗塞や心タンポナーデ、重症大動脈弁狭窄症(AS)では血圧低下のリスクが高いため禁忌または慎重投与。 |
| カルペリチド (hANP :ハンプ®) | 【開始量】 0.0125~0.025 γ で開始。 【調整】 血圧を見ながら慎重に増量(0.05 γ程度まで)。 | 血管拡張作用に加え、利尿作用とNa排泄作用を併せ持つ。 | 【推奨の変更】2025年ガイドラインでは、低用量投与での予後改善効果は明らかでないとされ、ルーチンでの使用は推奨されていません(推奨クラスIIb~III)。 |
| カルシウム拮抗薬 (ニカルジピン:ペルジピン®) | 【開始量】 ニトログリセリンでも降圧未達成であればニカルジピンを使用。 0.5~6 γ で開始。高濃度だと静脈炎を起こすので可能ならCVCから投与。 (例:10mg/10mLを生食希釈または原液で 3mL/h 程度から) 【調整】 血圧を見ながら 1~15 mL/h の間で調整。 | 主に動脈を強力に拡張させ、後負荷を下げる。硝酸薬で下がらない重症高血圧(CS1)で有効。 | 静脈拡張作用は弱いため、肺うっ血改善効果は硝酸薬に劣る場合がある。頻脈に注意。 |
血管拡張薬を使ってはいけないケース
血管を広げると血圧が下がるため、以下の状況では使用を控えるか、極めて慎重に行う必要があります。
• 低血圧・ショック状態(Cold): 収縮期血圧 < 90 mmHg(あるいは普段より著しく低い場合)では使用しません。
• 重症大動脈弁狭窄症(AS): 血管を広げすぎると、心臓から血液が出せずショックになるリスクがあります。
• 右室梗塞・心タンポナーデ: 前負荷(静脈還流)を維持する必要があるため、硝酸薬で血管を広げると致命的になることがあります。
【おまけ:Nohria-Stevenson分類の元論文、読んだことありますか?
これまでNohria-Stevenson分類という用語は知っていたものの元となった論文も知らなければ、どういった背景で誕生したかも知りませんでした。なぜこの分類が現在にいたるまで愛用(?)されているのか、元論文も読んでみました。
元論文は、「Nohria, A, Tsang, S, Fang, J. et al. Clinical assessment identifies hemodynamic profiles that predict outcomes in patients admitted with heart failure. JACC. 2003 May, 41 (10) 1797–1804.
https://doi.org/10.1016/S0735-1097(03)00309-7」です。
2003年にJournal of the American College of Cardiologyで発表されたNohriaらによるこの研究は、現在我々が日常的に使用している「Nohria-Stevenson分類」の基礎となった論文です。
この研究の最大の目的は、スワンガンツカテーテルなどの侵襲的な検査を行わなくとも、ベッドサイドでの身体所見だけで心不全患者の予後を予測できるかを検証することでした。Nohriaらは、入院した心不全患者452名を対象に、医師が身体診察で「うっ血の有無(WetかDryか)」と「組織灌流の状態(WarmかColdか)」を評価し、4つの臨床プロファイル(A、B、C、L)に分類しました。

結果として、このシンプルな分類は強力な予後予測因子になることが明らかになりました。1年後の死亡または緊急心臓移植のリスクを追跡したところ、うっ血も低灌流もない「Profile A(Dry-Warm)」の患者と比較して、うっ血がある「Profile B(Wet-Warm)」ではリスクが約2倍、うっ血と低灌流が合併した「Profile C(Wet-Cold)」ではリスクが約2.5倍から3.7倍に跳ね上がることが示されました。
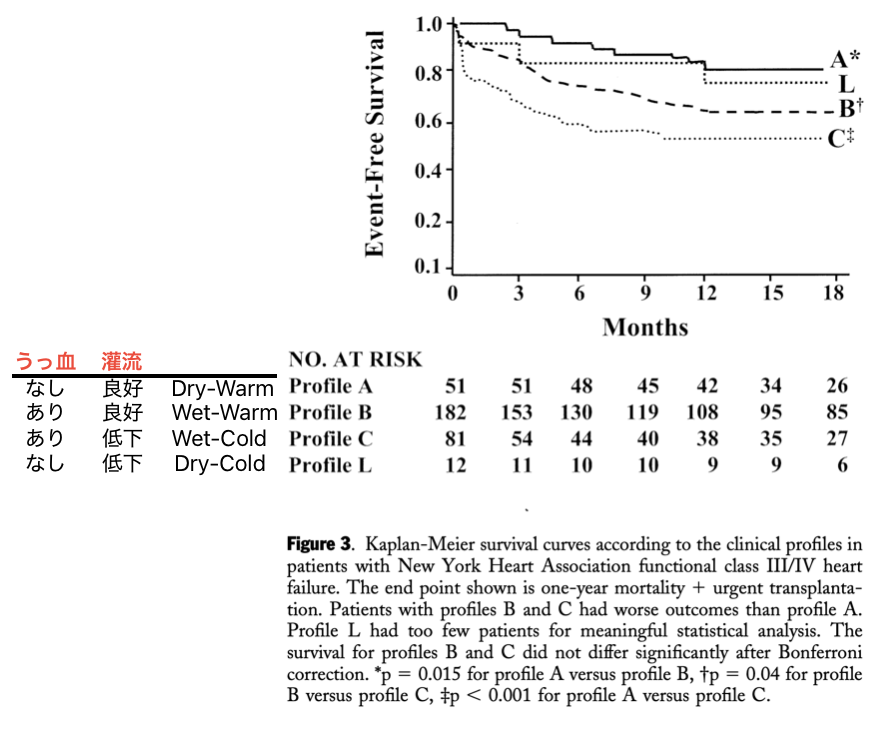
特筆すべき点は、この分類が患者の自覚症状(NYHA分類)以上に客観的な指標となり得るということです。たとえ患者が「息が苦しい」と訴え、NYHA分類でIII度やIV度と判定されるような重症感のある状態であっても、身体所見が「Profile A(Dry-Warm)」であれば、その後の予後は比較的良好であることが分かったのです。逆に、自覚症状と身体所見の乖離がある場合、身体所見に基づいたリスク評価の方が信頼性が高い可能性を示唆しています。
また、この臨床プロファイルが単なる主観的なものではなく、実際の血行動態を反映していることも裏付けられています。一部の患者で行われたカテーテル検査との比較では、「Wet」と判定された患者は肺動脈楔入圧(PCWP)が有意に高く、「Cold」と判定された患者は心係数(CI)が低い傾向にありました。つまり、聴診や触診といった基本的な診察技術が、カテーテル検査の代用として十分に機能し得ることが科学的に証明されたわけです。
結論として、この論文は「聴診器と手」があれば、高度な医療機器がない環境でも心不全の血行動態を推測し、適切な治療方針(利尿薬中心か、強心薬が必要かなど)を決定できることを示しました。
参考文献
- Nohria, A, Tsang, S, Fang, J. et al. Clinical assessment identifies hemodynamic profiles that predict outcomes in patients admitted with heart failure. JACC. 2003 May, 41 (10) 1797–1804.
https://doi.org/10.1016/S0735-1097(03)00309-7 - 2025年改訂版 心不全診療ガイドライン
- UpToDate – Approach to diagnosis and evaluation of acute decompensated heart failure in adults



コメント