- NPPVは気道に陽圧(EPAP/IPAP)をかけ、肺胞換気量の改善、酸素化の向上、および呼吸仕事量の軽減をもたらす人工呼吸管理方法です。
- 胸腔内圧の上昇により右室前負荷と左室後負荷を減少させるため、急性心原性肺水腫などの心不全病態において有利な血行動態の変化をもたらします。
- エビデンスに基づく主な適応(第一選択)は、COPD急性増悪、急性心原性肺水腫、免疫不全患者の急性呼吸不全などです。
- 一方で、自発呼吸の停止、血行動態の不安定、気道保護の不能、大量の気道分泌物、顔面外傷などは禁忌(気管挿管の適応)となります。
- 開始後1〜2時間で血液ガスや臨床所見による効果判定を行い、改善が認められない場合は遅滞なく気管挿管へ移行することが予後改善の鍵となります
- SpO2低下時の動き方やCO2ナルコーシスについての記事、PF比の記事も参照いただければ幸いです。
NPPVの適応
一般的な適応基準
酸素投与などの標準的な治療を行っても十分な改善が得られず、以下の基準を満たすような急性呼吸不全の患者が対象となります。
- 呼吸困難と呼吸仕事量の増加: 呼吸補助筋の使用や、腹部の奇異呼吸(吸気時に腹部がへこむ)を伴う中等度〜重度の呼吸困難。
- 頻呼吸: 呼吸数が1分間に24回以上(拘束性障害では30回以上)。
- 血液ガス異常:
- Ⅰ型呼吸不全: 酸素化の低下(PaO2 / FIO2 < 200)
- Ⅱ型呼吸不全: 呼吸性アシドーシス(pH < 7.35 かつ PaCO2 > 45 mmHg)。
・COPDの急性増悪: 呼吸性アシドーシスを伴う場合、NPPVは最も良い適応であり標準治療として強く推奨されます。
• 急性心原性肺水腫: 早期に開始することで挿管率や死亡率を有意に低下させます(主にCPAPを使用)。
• 免疫不全患者の急性呼吸不全: 血液悪性疾患、臓器移植後、ステロイド使用中などの患者において、気管挿管に伴う感染症リスク(VAPなど)を回避することで予後を改善します。
• COPD患者などの抜管およびウィーニング: 人工呼吸器からの早期離脱を支援し、再挿管を防ぐために用いられます。
• 慢性呼吸不全(在宅NPPVなど): 神経筋疾患、拘束性胸郭疾患(肺結核後遺症、脊椎後側彎症など)、肥満低換気症候群、慢性心不全に伴うチェーンストークス呼吸などにおいて、肺胞低換気を改善し生命予後やQOLを向上します。
NPPVの有効性を示唆するデータはあるものの、失敗した場合は速やかに気管挿管へ移行する必要があります。
• 気管支喘息の急性発作: 呼吸困難や呼吸機能を改善する可能性がありますが、急激に悪化することがあるため、挿管の遅れに注意が必要です。
• 胸部外傷: 肋骨骨折やフレイルチェストなどで、合併症を併発せずに酸素化を改善できる場合があります。
• 術後呼吸不全: 腹部手術や胸部手術、心臓血管手術後の無気肺や低酸素血症の予防・治療に有効な場合があります。
• DNI(挿管拒否)患者や終末期の緩和ケア: 挿管を希望しない高齢者や、進行がん・終末期患者に対する呼吸困難の緩和目的としても使用されます。
• ARDSや、心肺疾患を持たない重症肺炎
約半数でNPPVが失敗し、気管挿管の遅れが予後を悪化させるリスクがあるため、原則として気管挿管下の人工呼吸管理が基本となります(ごく軽症例などを除き、慎重な判断が必要です)
NPPVの禁忌
1. 絶対的禁忌(直ちに気管挿管等が必要、または物理的に実施不可能な状態)
| 状態・病態 | 理由・補足 |
|---|---|
| 心停止・呼吸停止、または緊急の気管挿管の必要性 | 自発呼吸がない、あるいは重度の呼吸促迫や不安定な不整脈などがあり、一刻も早い確実な気道確保と人工呼吸が必要なため。 |
| マスクの装着不可 | 顔面の重度の外傷や熱傷、骨折などで、マスクを密着させて陽圧をかけることが物理的に不可能なため。 |
2. 相対的禁忌(原則避けるべきだが、状況により慎重な適用や例外が考慮される状態)
| 状態・病態 | 理由・補足 |
|---|---|
| 血行動態の不安定 | ショック状態、持続する低血圧、未治療の重篤な不整脈などがある場合、陽圧換気(胸腔内圧の上昇)が心拍出量をさらに低下させる恐れがあるため。 |
| 意識障害(GCS 10未満など)、興奮・不穏、非協力的 | マスクに耐えられない、あるいは気道を自力で守れないため。ただし、「CO2ナルコーシスによる意識障害」の場合は例外であり、NPPVの換気によってCO2が排出されると速やかに意識が改善することが多いため、厳重なモニタリング下で試みられます。 |
| 気道保護の不能、大量の気道分泌物(喀痰)、嚥下障害 | 咳が弱い、痰が多すぎる、活発な嘔吐がある場合などは、マスク内で吐物や分泌物が詰まり、誤嚥性肺炎や窒息を引き起こすリスクが非常に高いため。 |
| 著しい気道閉塞 | 喉頭の腫瘤や気管腫瘍などによる物理的な気道閉塞はNPPVでは解除できず、気管チューブや気管切開などで閉塞部をバイパスする必要があるため。 |
| 顔面・頭部の外傷、手術、変形 | マスクの圧迫が創部の悪化(骨折の不安定化や気脳症など)を招いたり、激しい痛みや空気漏れを引き起こすため(軽度の軟部組織損傷などであればマスクの種類を変えて対応可能な場合もあります)。 |
| 最近の上気道、または食道・胃(上部消化管)の吻合・手術 | 胃や食道に空気が送り込まれて内圧が上がり、手術の縫合部(吻合部)が破綻(離開)するリスクがあるため。 |
| 活動性の上部消化管出血、腸管閉塞 | 消化管に空気が入ることで腹部膨満や嘔吐を誘発し、吐血や腸管内容物を誤嚥するリスクが高まるため。 |
| ドレナージされていない気胸 | 肺に陽圧をかけることで、漏れた空気が胸腔内に溜まり続け、「緊張性気胸」へと悪化する危険があるため。※事前に胸腔ドレーンを挿入してドレナージがされていればNPPVは可能です。 |
| 急性に生命を脅かす非呼吸器系の臓器不全 | 呼吸不全だけでなく、多臓器不全などの重篤な全身状態に陥っている場合はNPPV単独での管理は難しく、確実な気道・呼吸管理(挿管)が推奨されます。 |
| 長期間(4〜7日以上)の機械換気が必要と予想される場合 | NPPVは一般的に1〜3日程度の短期的なサポートとして位置づけられており、長期化する場合は挿管管理の方が安全性が高いため。 |
| 複数の禁忌事項が重複している場合 | 相対的禁忌であっても、複数が当てはまる場合はリスクが高すぎるため、早期の抜管を見据えたうえで気管挿管を行うことが推奨されます。 |
このように、単に「使えない」というだけでなく、「気道を守れるか(誤嚥しないか)」「マスクからの圧力が悪影響を及ぼさないか(気胸や縫合部)」「患者の協力が得られるか」という観点から禁忌が設定されています。
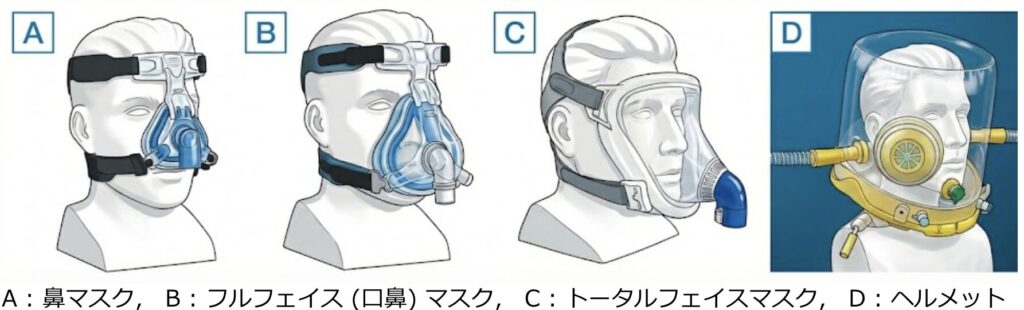
インターフェースの種類
| インターフェースの種類 | メリット | デメリット |
|---|---|---|
| 鼻マスク (鼻のみを覆う) | ・誤嚥の危険性が少ない ・痰などの分泌物の処理がしやすい ・装着したまま会話や食事が可能 ・顔を覆う面積が少なく、閉塞感・不快感が少ない ・顔にフィットしやすい | ・口から空気が漏れやすい(口呼吸の患者には不向き) ・鼻づまり(鼻閉)がある場合は効果が低下する ・鼻根部に発赤や皮膚潰瘍ができやすい |
| フルフェイスマスク(口鼻マスク) | 口からの空気漏れを防げる 口呼吸をしている患者にも有効 | ・嘔吐時や痰が多い場合、誤嚥や窒息のリスクが高まる ・装着中は会話や食事が難しい ・閉塞感が強い ・顔の骨格に合わせたフィットが難しい ・食道・胃へ空気が流れ込みやすく、腹部膨満を起こしやすい |
| トータルフェイスマスク (顔全体を覆う) | ・頬のくぼみなどで鼻マスクやフルフェイスマスクが合わない(空気が漏れる)場合でも対応できる ・鼻根部の潰瘍形成などの局所的な皮膚障害を予防できる | ・装着中は会話や食事ができない ・嘔吐時の誤嚥リスクがある ・マスク内の死腔(換気に関与しない無駄な空間)が大きくなりやすい |
| ヘルメット (頭部全体を覆う) | ・顔面への圧迫がないため、顔面の皮膚障害を完全に回避できる ・閉所恐怖症を最小限に抑えられ、患者の忍容性が良好な場合がある | ・内部の容積が大きいため、患者が吐いたCO2の再呼吸(蓄積)が起こりやすい ・機械と患者の呼吸のタイミングがズレやすい(非同調) ・気流による内部の騒音が大きい ・固定用ベルト(脇の下を通す)により、腕の浮腫が生じることがある |
臨床現場での使い分けのポイント
• 基本は「鼻マスク」か「フルフェイスマスク」: 急性期・慢性期(在宅)を問わず、実際の臨床現場ではこの2種類がほとんどを占めます。
• 急性期はフルフェイスから: 急性呼吸不全で呼吸が苦しい時は口呼吸になっていることが多いため、最初は口からの空気漏れを防げるフルフェイス(鼻口)マスクが第一選択となることが多いです。
• 状態が落ち着いたら鼻マスクへ: 患者さんがNPPVの風に慣れ、状態が安定してきたら、会話や食事が可能で不快感の少ない鼻マスクへの変更を検討します。
• 皮膚障害対策としてのローテーション: 長時間同じマスクを装着していると特定の部位に皮膚潰瘍ができるため、睡眠時は口漏れを防ぐフルフェイスマスクやトータルフェイスマスク、覚醒時は鼻マスクといったように、種類の違うマスクをローテーションすることも皮膚障害の予防に有効です。
モード
bilevel PAP(二相式気道陽圧)とは?
bilevel PAPは、「吸気時と呼気時で、異なる2つの圧力を設定する換気方式」の総称です。
• IPAP(吸気圧):息を吸うときに高い圧力をかけて呼吸を助ける。
• EPAP(呼気圧):息を吐くときに低い圧力をかけて気道が開いた状態を保つ。
この「2段階の圧力をかける」という仕組みそのものをbilevel PAPと呼びます。
IPAPを高くするメリットは?
IPAPを高くする最大のメリットは、「プレッシャーサポート(吸気補助)」が大きくなり、1回換気量の増加と呼吸仕事量(呼吸の労力)の軽減が得られることです。
具体的には以下のような効果とメリットがあります。
• 1回換気量が増える: IPAPとEPAP(呼気圧)の差が「プレッシャーサポート」として働くため、IPAPを高くしてこの差を大きくすることで、1回の呼吸でより多くの空気を肺に送り込むことができます。1回換気量が低い状態の改善に有効です。
• 息がラクになる(呼吸仕事量の軽減): 機械が強く息を吸う手助けをしてくれるため、患者さん自身の吸気努力(呼吸仕事量)が減ります。適切な設定になれば、患者さんの異常に多かった呼吸回数が低下し、実際に「息がラクになった」と感じることができます。
※注意点(高くしすぎるデメリット) IPAPはむやみに高くすれば良いというわけではありません。下部食道の圧はおよそ20 cmH2Oであるため、IPAPが20 cmH2Oを超えると胃へ空気が流れ込む(呑気)という問題が起こりやすくなります。そのため、20 cmH2Oを超えるような高いIPAPが必要な場合は、いたずらにNPPVで粘らず、より確実に呼吸を補助できる気管挿管と人工呼吸器への切り替えを考慮する必要があります
EPAPを高くするメリットは?
1. 酸素化の改善と呼吸仕事量の軽減
主に心原性肺水腫など、低酸素血症があり胸部X線で「肺が白くなっている状態」で得られるメリットです。 息を吐くときにも圧力をかけることで、機能的残気量(FRC)を増大させます。これにより、ペシャンコに潰れていた肺胞が内側から押し広げられてシャント(無駄な血流)が減り、酸素化が改善します。同時に、肺が膨らみやすくなる(コンプライアンスが改善する)ため、患者さんが息をするための労力(呼吸仕事量)を低下させる効果があります。 この目的の場合、患者さんの状態を見ながら5〜10 cmH2O程度に設定されることが多いです。
2. 息の吸い始めにくさの軽減(オートPEEPの軽減)
主にCOPD(慢性閉塞性肺疾患)の急性増悪など、「閉塞性肺疾患」がある場合で得られるメリットです。 COPDの患者さんは、息を十分に吐ききれずに肺の中に空気が残ってしまう「オートPEEP」という状態になりやすく、これが原因で次の息が吸い始めにくくなります。EPAPで外側から圧力をかけることで、このオートPEEPによる息の吸い始めにくさを軽減させることができます。
※注意点(高くしすぎるデメリット)
COPDなどの閉塞性肺疾患に対してEPAPを高くしすぎると、肺が膨らみすぎる「過膨張」を悪化させてしまい逆効果になります。そのため、この目的で使用する場合は、オートPEEPを超えないように5 cmH2O程度に留めるよう設定します。 また、低酸素血症の改善が目的であっても、あまりに高い圧を必要とする場合はそれだけ肺の状態が悪いということになるため、気管挿管して人工呼吸器を開始する方が良いとされています
S/Tモードとbilevel PAPのちがいは?
S/Tモードは、上記のbilevel PAP方式のなかで選択できる「具体的な換気モードの1つ」です。
bilevel PAP方式の機器では、患者さんの呼吸にどのように合わせるかによって、主に以下の3つのモードが選べます。
• S(Spontaneous:自発)モード 患者さんの自発呼吸に完全に合わせるモードです。患者さんが吸い始めたらIPAP、吐き始めたらEPAPに切り替えます。
• T(Timed:調節)モード 患者さんの呼吸に関係なく、機械があらかじめ設定した回数とタイミングで強制的にIPAPとEPAPを切り替えます。
• S/Tモード(Spontaneous/Timedモード) 上記2つの「いいとこ取り」をしたモードです。 基本はSモードとして患者さんの自発呼吸に合わせて圧力を変化させますが、もし患者さんの呼吸が一定時間止まった(無呼吸になった)場合には、安全のためのバックアップとして自動的にTモードに切り替わり、機械が強制的に圧力を送って呼吸をさせます。
つまり、「bilevel PAPという換気方式(吸気と呼気で圧を変える仕組み)を使って、S/Tモード(自発呼吸に合わせつつ、止まったらバックアップする設定)で呼吸をサポートする」というのが正しい表現になります
グラフをみながら換気モードを理解する
わかりやすい図を引用させていただきました(https://www.kango-roo.com/learning/3502/ )。
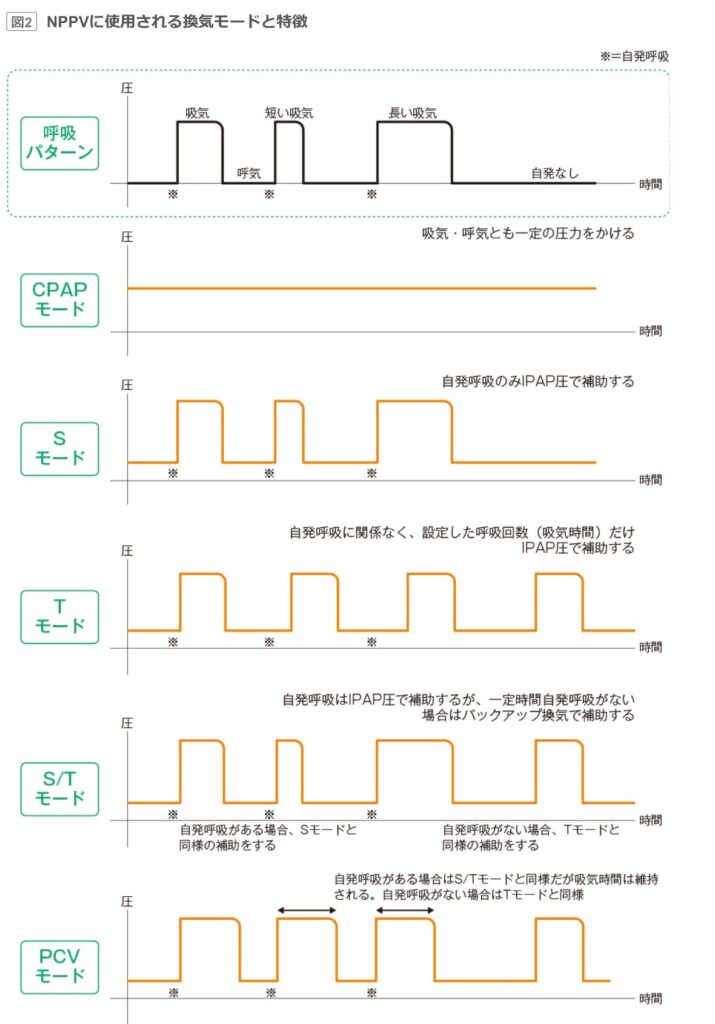
図の中では同じような四角い波形で描かれているため直感的に同じものに見えてしまうのですが、この図の読み解き方には重要なポイントがあります。
- 一番上の「呼吸パターン」:患者さんの「吸気努力のタイミングと長さ」を示すタイムライン これは人工呼吸器の「圧」ではなく、患者さんが「いつ、どのくらいの長さで息を吸おうとしているか(※=自発呼吸)」を示すための単なる基準となるモデルです。人間の本来の呼吸は胸腔内を陰圧にして空気を引き込むため、生理学的に言えばこの波形は「患者さん自身の吸気努力(陰圧)」を便宜上図式化したものになります。
- そのほかの波形は、機械が人為的に気道へ押し込む「プラスの圧力」です。
- つまり、この図は「患者さんの自発呼吸(タイミングと長さ)に対して、機械側の各モードがどのようにIPAP(陽圧)を合わせているか」を比較するためのものです。
- それぞれのモードが、患者さんの「呼吸パターン」に対してどうIPAPを出しているかを見比べると、非常にわかりやすいです。
- Sモード(Spontaneous): 一番上の波形で患者さんが息を吸い始めた瞬間(※印)を感知して、IPAPを開始します。患者さんが「短い吸気」なら短く、「長い吸気」なら長く、患者さんのリズムに完全に同調してIPAPをかけています。
- Tモード(Timed): 一番上の「呼吸パターン(患者の努力)」を完全に無視しています。患者さんが息を吸おうが吸うまいが関係なく、あらかじめ設定した時間と回数に従って、機械のペースで規則正しく強制的にIPAPをかけています。
- S/Tモード(Spontaneous/Timed): 基本はSモードのように患者さんの「呼吸パターン」に合わせてIPAPをかけます。しかし、右側のように患者さんの呼吸が一定時間止まった場合(自発なし)には、安全のためにTモードの機能が発動して強制的にIPAPをかけています(バックアップ換気)。
病態にあわせたモード設定
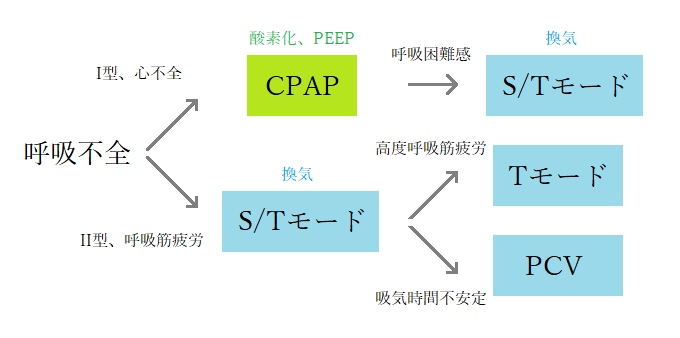
酸素化に問題があるI型呼吸不全、PEEPが必要な心不全 =【CPAP】
- I型呼吸不全への効果:I型呼吸不全は、呼吸そのもの(換気)はできているものの、肺にうまく酸素を取り込めない状態です。CPAPで常に一定の陽圧(PEEP)をかけ続けることで、ペシャンコに潰れた肺胞を押し広げて(無気肺の改善・防止)、酸素を取り込みやすくします。
- 心不全への効果:急性心原性肺水腫などの心不全では、肺に水が溜まって酸素化が悪化します。CPAPによる陽圧は、肺の水分を血管に押し戻すだけでなく、胸腔内の圧力を上げることで心臓に返ってくる血液量(前負荷)や心臓が血液を送り出す際の抵抗(後負荷)を減らし、弱った心臓の働きを助ける効果があります。そのため、心不全にはCPAPが第一選択とされています。
II型呼吸不全や努力呼吸が強い場合 =【S/Tモード(bilevel PAP)】
- 換気補助と二酸化炭素の排出:II型呼吸不全(COPDの増悪など)は、肺胞での換気が不十分になり、体内に二酸化炭素が蓄積している状態です。S/Tモードで息を吸うときに高い圧力(IPAP)をかけることで、肺にしっかり空気を送り込み(換気補助)、二酸化炭素の排出を促します。
- 呼吸筋の休息(努力呼吸の軽減):呼吸困難が強く、肩や首の筋肉まで使って一生懸命呼吸をしている(努力呼吸)患者さんは、呼吸筋が疲労困憊しています。S/Tモードの吸気補助は、患者さんの「吸う労力」を機械が肩代わりしてくれるため、呼吸仕事量を減らして呼吸筋を休ませる効果があります。また、S/Tモードは患者さんの呼吸が弱くなったり止まったりした際に、バックアップとして機械が強制的に換気を行ってくれるため、安全性が高いのも特徴です
各疾患・病態のNPPVの設定
病態や疾患ごとのNPPVの設定方法について、主に「心原性肺水腫などの低酸素血症(白い肺)」と「COPDなどの閉塞性肺疾患(PaCO2上昇)」の2つに大別しています。
心原性肺水腫など、低酸素血症がメインの病態(白い肺)
ショックを合併していない心原性肺水腫による急性呼吸不全では、CPAPが第一選択となります。
- モード:CPAP
- CPAPの設定: 5〜10 cmH2O
- 目的: 機能的残気量(FRC)を増大させることでシャントを減らして酸素化を改善し、同時に肺のコンプライアンスを改善して呼吸仕事量を低下させます。
- あまりに高い圧を要する場合は、気管挿管への移行を検討します。
COPD急性増悪など、PaCO2上昇を伴う閉塞性肺疾患
換気に手助けが必要なCOPD急性増悪や、PaCO2上昇を伴う呼吸不全では、S/Tモードが第一選択となります。
- モード: S/T
- IPAP(吸気圧)の設定: EPAP + 5〜10 cmH2O
- EPAP(呼気圧)の設定: 5 cmH2O程度
- 目的: 閉塞性肺疾患特有の「オートPEEP」に打ち勝ち、息を吸い始めやすくするためです。
- あまり高い圧をかけると肺の過膨張を悪化させるため、オートPEEPを超えない5 cmH2O程度に設定します。
その他の設定やコツ
- 初期設定のコツ
- はじめから目標の圧力をかけるのではなく、まずは患者が慣れるまで低い圧から開始します。
- 目安として、CPAPなら4 cmH2O程度、Bi-level PAPならIPAP 8 cmH2O / EPAP 4 cmH2O程度で開始し、患者が慣れるにしたがって徐々に圧を上げます。
- 最初はストラップで固定せず、手でマスクを押さえて様子を見るのが重要です。
- ライズタイム
- ライズタイム(圧の立ち上がり時間)とは、簡単に言うと「患者さんが息を吸い始めた瞬間から、機械が目標の圧力(IPAP)まで圧を上げるのにかかるスピード」のことです。
- PCV(従圧式調節換気)やプレッシャーサポート(PS)におけるライズタイムと全く同じ考え方で、人工呼吸器から送られてくる風が「フワッ」とゆっくり来るか、「ドンッ」と急に来るかを決める設定になります。
- 患者さんが勢いよく息を吸っているとき: 風がゆっくり来ると「息が吸い足りない」と苦しくなってしまうため、より早く目標の圧力(IPAP)に到達するように(立ち上がりを早く)設定します。
- 患者さんがゆっくり息を吸っているとき: 風が急に来ると「圧迫感があって不快」と感じてしまうため、時間をかけて目標の圧力(IPAP)に到達するように(立ち上がりを遅く)設定します。
- 呼吸回数(S/Tモードの場合): NPPVでの呼吸回数設定はあくまで「バックアップ」です。気管チューブがないNPPVでは、患者の吸気努力がない時に圧をかけても上気道や声門が開いているとは限らないため、呼吸回数の設定をむやみに増やしてもPaCO2を下げる効果は期待できません。
具体的なバンド調整の仕方は?
リークを最小限にしつつ、患者の苦痛や皮膚障害を防ぐための具体的なバンド(ストラップ)調整の手順とコツは以下になります。個人的には十分な説明と、軽いマスクフィッティングがコツだと思ってます。説明なしにいきなりバンドを巻くと協力が得られなくなり余計に苦しませてしまうといった経験があります。
バンド調整の具体的なステップ
1. まずは「手」でマスクを当てる いきなりバンドで顔に固定するのではなく、最初は手でマスクを顔にそっと当てて保持し、換気を開始します。患者が機器からの風に慣れ、自身の呼吸と機械の送気が同調するのを待ちます。
2. かなり「緩め」に仮止めする 呼吸と機械が合ってきたら、まずはバンドをかなり緩めの状態にして仮固定します。
3. 「左右対称」に少しずつ締めていく 「まだ緩いので少しずつ締めていきますね」と患者に声をかけながら、大きな空気漏れ(目元などへの不快な漏れ)がなくなる「ちょうどいい塩梅」まで徐々にバンドを締めていきます。このとき、左右均等な力で締め、上下にもズレていないか確認することが隙間を作らないポイントです。
4. ズレの確認(会話テストなど) 鼻口マスクを使用している場合、患者に少し会話をしてもらい、顎が動いてもマスクの位置がズレたり外れたりしないかを確認します。
調整時の重要な注意点・コツ
• 「締めすぎ」は逆効果 リークをなくそうとしてバンドを強く締めすぎると、皮膚やマスクのクッションが過度に圧迫されてシワやよれが生じ、かえってそこが新たな隙間となってリークの原因になります。また、締めすぎは鼻の付け根などの皮膚の潰瘍や不快感を直接的に引き起こすため、過度な締め付けは禁物です。
• 「ゼロ」を目指さない NPPVには構造上必ず意図的なリークが発生します。機械が患者の呼吸としっかり同調しており、換気量や酸素飽和度(SpO2)が保たれているのであれば、ある程度のリーク(おおむね40L/分以下。文献によっては60Lとしていますが、私の施設では40としています)は許容し、それ以上きつく締める必要はありません
NPPV開始後の効果判定はいつ行うべきか?
- NPPV開始後の効果判定は、開始後1〜2時間で行うべきです。特に高二酸化炭素血症がある患者さんの場合は、このタイミングで以下の評価を行います。
- 呼吸状態の観察:呼吸回数や心拍数が改善しているか、患者さんの呼吸がラクになっているか(呼吸仕事量の軽減)を確認します。
- 血液ガスの測定:開始後1〜2時間で血液ガスを測定し、ガス交換(酸素化や二酸化炭素の排出)が実際に改善しているかを客観的に評価します。
NPPVが成功するかどうかの予測において、「NPPV開始後に改善する」という点が最も重要です。そのため、この開始1〜2時間後の評価で状態がよくならない場合は、いたずらにNPPVを継続するのではなく、速やかに気管挿管と人工呼吸器への切り替えを検討する必要があります。
NPPVの離脱基準は?
■NPPVからの離脱には、すべての疾患に共通する「これ」という絶対的な数値基準があるわけではありませんが、私は概ね以下のような臨床所見や検査データの改善を目安としています。
• 自他覚症状の改善: 呼吸困難感や喘鳴などが明らかに軽減している。
• バイタルサインの安定: 頻呼吸や頻脈が改善している。
• 血液ガスの改善:
◦呼吸性アシドーシス(pHの低下やPaCO2の蓄積)が改善・消失している。
◦ 酸素化が安定している(例:少ない酸素投与量でPaO2 > 60 mmHgや、目標のSpO2を維持できている)。
• 基礎疾患の改善: COPDの急性増悪や心不全など、呼吸不全を引き起こした原因が治療により改善・解消に向かっている。
■実際の離脱ステップ
• 最初から完全に外すのではなく、食事や休憩などのタイミングで一時的にNPPVを外し、酸素吸入のみにして様子を見ます。外す時間を日中から徐々に増やしていく方法をとっています。
• 外している間のバイタルサイン、SpO2、血液ガスをチェックします。呼吸困難が悪化したり数値が低下するようであれば速やかにNPPVを再装着し、数時間経過しても安定していれば完全に離脱可能と判定します。
参考文献
- Chaudhuri D, Trivedi V, Lewis K, Rochwerg B. High-Flow Nasal Cannula Compared With Noninvasive Positive Pressure Ventilation in Acute Hypoxic Respiratory Failure: A Systematic Review and Meta-Analysis. Crit Care Explor. 2023 Mar 28;5(4):e0892. doi: 10.1097/CCE.0000000000000892. PMID: 37007904; PMCID: PMC10060083.
- Carron, M., U. Freo, A. S. BaHammam, et al. “Complications of Non-Invasive Ventilation Techniques: A Comprehensive Qualitative Review of Randomized Trials.” British Journal of Anaesthesia 110, no. 6 (2013): 896–914.
- Rezoagli, Emanuele, Alice Nova, Guillaume Carteaux, et al. “A Clinical Guide to Non-Invasive Respiratory Support in Acute Respiratory Failure: Ventilation Settings, Technical Optimization and Clinical Indications.” Critical Care 29, no. 1 (2025): 496.
- Noninvasive ventilation in adults with acute respiratory failure_ Benefits and contraindications – UpToDate(2026/02/24閲覧)
- https://www.kango-roo.com/learning/3502/ (2026/02/25閲覧)
- https://ce7meliteracy.com/archives/755 (2026/02/25閲覧)



コメント