代謝性アルカローシスは、血清重炭酸イオン(HCO3–)濃度と動脈血pHが上昇する病態です。この病態のメカニズムを理解する上で極めて重要なのは、アルカローシスの「発生」(重炭酸イオンの増加)と、それが腎臓で適切に排泄されずに「維持」されるという2つのステップが必要である点です。
正常な腎機能を持つ人は、余分な重炭酸イオンを尿中に急速に排泄できるため、代謝性アルカローシスは通常持続しません。これが持続するためには、循環血液量減少(低容量)、有効動脈血液量の減少(心不全や肝硬変など)、クロール(Cl)欠乏、低カリウム血症、または糸球体濾過量(GFR)の低下などにより、腎臓での重炭酸イオン排泄能力が低下(維持フェーズ)している必要があります。
代謝性アルカローシスを発生させる主な原因とメカニズム
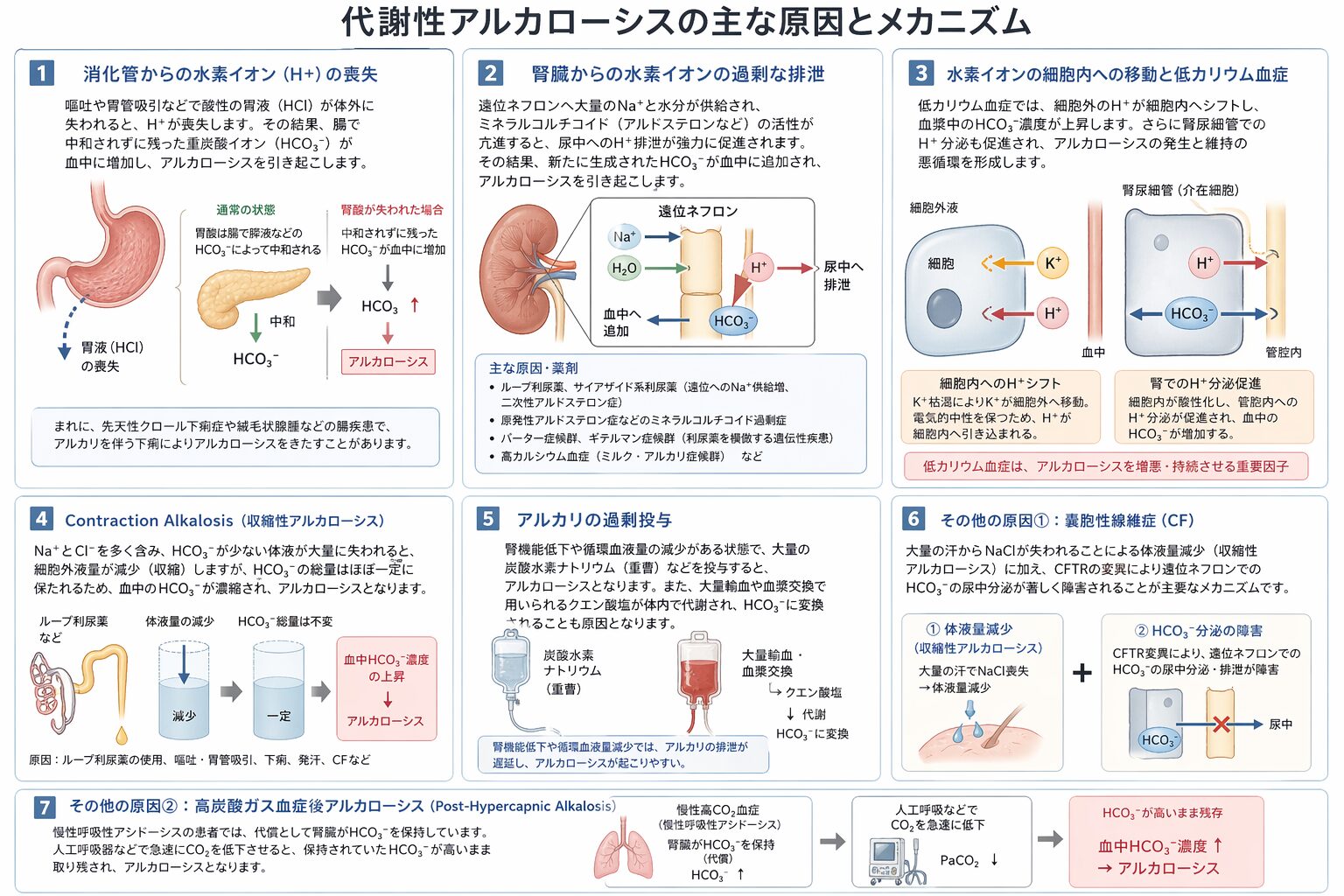
消化管からのH+の喪失
胃液には高濃度の塩酸が含まれています。嘔吐や胃管吸引などによって酸性の胃液が体外に失われると、H+が喪失します。正常であれば胃酸は腸で膵臓などから分泌される重炭酸イオンによって中和されますが、胃酸が腸に到達しないため、過剰となった重炭酸イオンが血中に残り、アルカローシスを引き起こします。これが最も一般的な原因の一つです。また、極めて稀ですが、先天性クロール下痢症や絨毛状腺腫などの腸疾患でも、塩化物イオンの吸収と重炭酸イオンの分泌を担う交換輸送体の障害などによって、大量のアルカリを伴う下痢が生じ、アルカローシスを引き起こすことがあります。
H+が減っても、Cl–が減っても、いずれの場合でも代謝性アルカローシスになる
水素イオン(H+)の減少とクロール(Cl–)の減少は、いずれも代謝性アルカローシスを引き起こす根本的な原因となります。さらに言えば、体内の酸塩基平衡において、これら2つの減少は表裏一体の現象として密接に関連しています。
それぞれの視点からアルカローシスになる理由と、その関係性は以下の通りです。
- H+(酸)の減少によるメカニズム
- 胃液や尿としてH+が体外へ失われたり、低カリウム血症によって細胞外のH+が細胞内へ移動したりすることで、血液中のH+が減少します。
- 体内では常に「H2O+CO2→ H+ + HCO3–」という反応が起きていますが、H+が喪失すると、ペアとして生成されたアルカリであるHCO3–だけが体内に取り残されて蓄積し、アルカローシスを引き起こします。
- Cl–の減少によるメカニズム(電気的中性の維持)
- 細胞外液(血液など)の陰イオンの大部分はCl–とHCO3–で構成されています。
- 利尿薬の使用やCl–を多く含む腸液の喪失などによってCl–が失われると、体は電気的なプラスマイナスのバランス(電気的中性)を保つために、もう一つの陰イオンであるHCO3–を代償的に増やして穴埋めをします。その結果、HCO3–が増加してアルカローシスとなります。
H+の減少とCl–の減少は同時に起こりやすい
臨床的に非常に重要な点として、H+の喪失とCl–の喪失は別々に起こるだけでなく、同時に起こることが非常に多いという特徴があります。
- 嘔吐や胃管吸引: 胃酸の主成分は塩酸(HCl)です。胃液が体外へ失われるということは、H+とCl–を一緒に捨てていることになります。
- 腎臓からの酸排泄: 腎臓から酸(H+)を尿中に捨てる際にも、しばしば塩化アンモニウム(NH4Cl)の形で排泄されるため、ここでもH+とCl–が同時に失われます。
このように、代謝性アルカローシスが起きている細胞外液においては、「HCO3–の増加 = H+の低下(pH上昇) = Cl–の低下」という関係性が成り立ちます。したがって、H+が減った結果としてアルカローシスを考えることも、Cl–が減った結果としてアルカローシスを考えることも、どちらも病態の捉え方として正解であり、最終的に同じ状態に行き着きます。
腎臓からの水素イオンの過剰な排泄
腎臓の遠位ネフロンへ大量のナトリウムと水分が供給され、同時にその部位でミネラルコルチコイド(アルドステロンなど)の活性が亢進していると、尿中へのH+の排泄が強力に促進されます。これにより、腎臓内で新たに生成された重炭酸イオンが血中に追加されます。
- 主な原因疾患・薬剤: ループ利尿薬やサイアザイド系利尿薬の使用(遠位へのナトリウム供給増と二次性アルドステロン症を引き起こす)、原発性アルドステロン症などのミネラルコルチコイド過剰症、利尿薬の作用を模倣する遺伝性疾患であるバーター症候群やギテルマン症候群、高カルシウム血症(ミルク・アルカリ症候群)などが含まれます。
水素イオンの細胞内への移動と低カリウム血症
細胞外液のH+が細胞内にシフトすることでもアルカローシスは発生します。これは主に低カリウム血症の患者で起こります。
- メカニズム: カリウムが枯渇すると、カリウムが細胞内から細胞外へ移動し、電気的中性を保つために細胞外のH+が細胞内へと引き込まれます。これにより血漿中の重炭酸イオン濃度が上昇します。さらに、腎尿細管の細胞内が酸性になることで管腔内へのH+分泌が促進され、血中への重炭酸イオンの追加につながります。低カリウム血症は、アルカローシスの発生と維持の双方に悪循環をもたらす重要な要因です。
Contraction Alkalosis
ナトリウムとクロールを高濃度に含む一方で、重炭酸イオンの濃度が低い体液が大量に失われることで起こります。
- メカニズム: 例えば、ループ利尿薬によって大量の水分が失われると、細胞外液量は減少しますが、細胞外の重炭酸イオンの総量はほぼ一定に保たれるため、結果的に血液中の重炭酸イオンが濃縮されて濃度が上昇します。
アルカリの過剰投与
腎機能が低下している患者や循環血液量が減少している患者に、大量の炭酸水素ナトリウム(重曹)などを投与した場合に起こります。また、大量の輸血や血漿交換を受けた場合、抗凝固剤として含まれているクエン酸塩が体内で代謝されて重炭酸ナトリウムに変換されるため、アルカローシスの原因となります。
その他の原因
- 嚢胞性線維症 (CF): 大量の汗から塩化ナトリウムが失われることによる体液量減少(Contraction Alkalosis)に加え、CFTR(嚢胞性線維症膜コンダクタンス制御因子)の変異によって、遠位尿細管での重炭酸イオンの尿中への分泌排泄が著しく障害されることが主要な発生メカニズムです。
- 高炭酸ガス血症後アルカローシス: Post-Hypercapnic Alkalosisともいうようです。慢性呼吸性アシドーシスの患者は、代償として腎臓が重炭酸イオンを保持しています。人工呼吸器などで急速にCO2を低下させると、血中の重炭酸イオン濃度が高い状態のまま取り残され、アルカローシスとなります。
Post-Hypercapnic Alkalosis(PHA)について詳しく
■高炭酸ガス血症後アルカローシス(Post-Hypercapnic Alkalosis: PHA)とは、慢性的な呼吸不全(COPDや神経筋疾患など)による慢性高炭酸ガス血症の患者に対し、人工呼吸器などで換気を急速に改善させた際に生じる医原性の代謝性アルカローシスです。
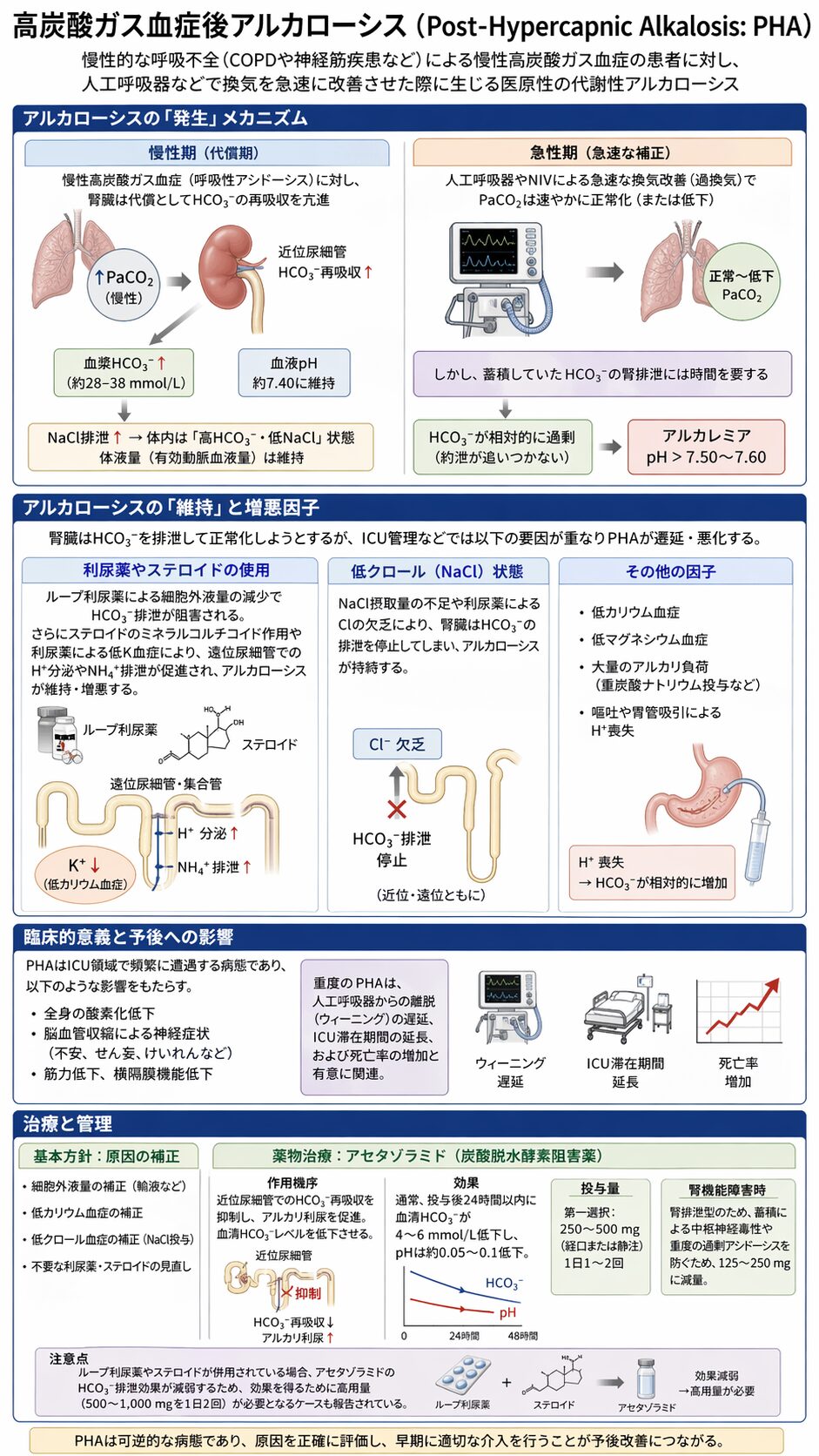
■ PHAの「発生」メカニズム
- 慢性期(代償期): COPDなどで慢性的な高炭酸ガス血症(呼吸性アシドーシス)があると、腎臓は代償機能として近位尿細管での重炭酸イオン(HCO3–)の再吸収を亢進させます。これにより血漿HCO3–濃度が上昇し、血液pHを正常付近(約7.40)に保ちます。この際、塩化ナトリウム(NaCl)の排泄が促進され、体内は「高HCO3–・低NaCl」の状態で体液量(有効動脈血液量)が維持されます。
- 急性期(急速な補正): 感染症の増悪などで急性呼吸不全に陥った患者に対し、人工呼吸器や非侵襲的換気(NIV)を導入して急速に換気を改善(過換気)させると、動脈血炭酸ガス分圧(pCO2)は速やかに正常化(または低下)します。しかし、蓄積していた血中HCO3–の腎臓からの排泄には時間がかかるため、正常化されたpCO2に対してHCO3-が過剰な状態となり、重篤なアルカレミア(pH > 7.50〜7.60)を引き起こします。
■ PHAの「維持」と増悪因子
高くなったHCO3–を排泄して正常化しようと腎臓は働きますが、実際のICU管理などでは、これまでに解説したような「維持フェーズ」の要因が重なることでPHAが遷延・悪化します。
- 利尿薬やステロイドの使用: 心不全やCOPD増悪の治療でループ利尿薬が投与されると、細胞外液量の減少を招き、HCO3–の排泄が阻害されます。さらに、ステロイドのミネラルコルチコイド作用や利尿薬によって低カリウム血症が引き起こされると、遠位尿細管でのH+分泌やアンモニウム排泄が促進され、アルカローシスがさらに維持・増悪します。
- 低クロール(NaCl)状態: 患者のNaCl摂取量が少ない場合や、利尿薬によってClが欠乏していると、腎臓はHCO3–の排泄を停止してしまい、アルカローシスが持続します。
■臨床的意義と予後への影響
PHAはICU領域で頻繁に遭遇する病態であり、全身の酸素化低下や神経症状を引き起こす可能性があります。重度のPHAは、人工呼吸器からの離脱の遅延、ICU滞在期間の延長、および死亡率の増加と有意に関連しているため、早期の介入が不可欠です。
■治療と管理
PHAの治療の基本は、アルカローシスを維持している原因(細胞外液量の減少、低カリウム血症、低クロール血症など)の補正です。 また、薬物治療としてアセタゾラミド(炭酸脱水酵素阻害薬)が有効な選択肢となります。
- 作用機序: 近位尿細管でのHCO3–再吸収を抑制し、アルカリ利尿を促すことで血清HCO3–レベルを低下させます。通常、投与後24時間以内に血清HCO3–が4〜6 mmol/L低下し、pHは約0.05〜0.1低下します。
- 投与量: 第一選択として250〜500 mg(経口または静注)を1日1〜2回投与します。ただし、腎排泄型であるため、腎機能障害患者では蓄積による中枢神経毒性や重度の過剰アシドーシスを防ぐため、125〜250 mgに減量する必要があります。
- 注意点: ループ利尿薬やステロイドが併用されている場合、アセタゾラミドのHCO3–排泄効果が減弱するため、効果を得るために高用量(500〜1,000 mgを1日2回)が必要となるケースも報告されています。
代謝性アルカローシスの鑑別には尿Cl–を使う
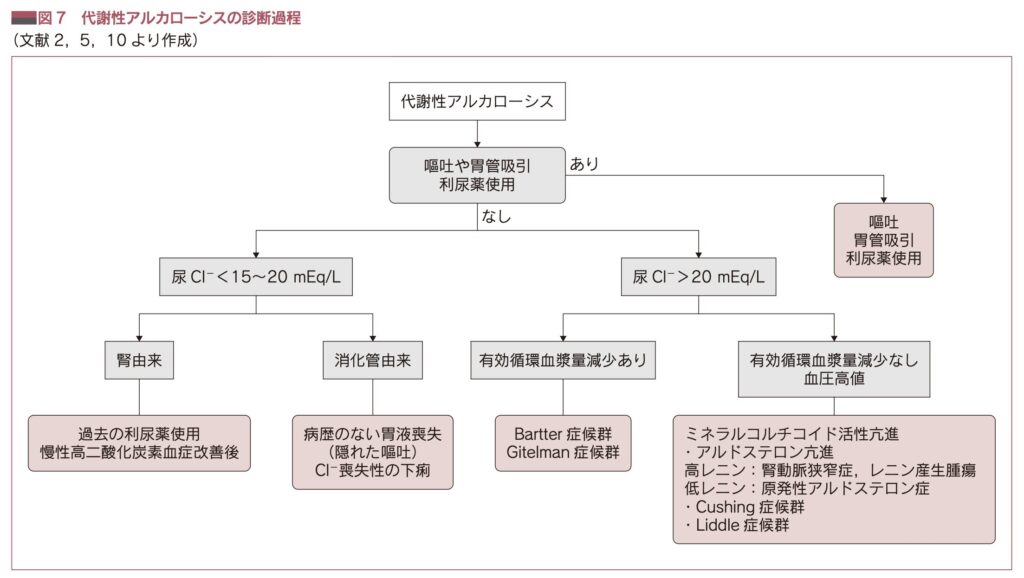
1. 尿中Cl– < 15〜20 mEq/L の場合(腎臓がCl–を保持しようとしている)
体内のCl–が著しく欠乏しており、腎臓が必死にCl–を再吸収して尿中に漏らさないようにしている状態です。生理食塩液などの補充で改善しやすい「Cl–反応性」のタイプです。
- 主な原因: 嘔吐や胃管吸引による胃液の喪失、過去の利尿薬使用、慢性高二酸化炭素血症改善後(PHA)、Cl–喪失性の下痢(消化管からの喪失)などが考えられます。
2. 尿中Cl- > 20 mEq/L の場合(尿中にCl-が漏れ出ている)
腎臓の異常によって尿中へCl-が不適切に排泄され続けているか、あるいは有効循環血漿量が保たれている状態です。
- 主な原因: バーター症候群やギテルマン症候群などが挙げられます。また、血圧が高く有効循環血漿量の減少がない場合は、原発性アルドステロン症やクッシング症候群といったミネラルコルチコイド活性の亢進(HCO3-が貯留するCl-不応性のタイプ)が強く疑われます。
尿検査を行うタイミングの重要な注意点
診断において非常に重要なのは、可能なかぎり早期に(治療介入前に)尿検査を提出して尿中Cl–を確認することです。
救急外来や病棟などでは、初期治療として生理食塩液(塩化ナトリウム)の輸液が開始されることがよくあります。輸液の開始後に検査が遅れてしまうと、補充されたCl–によって体内のバランスがすでに「回復過程」に入ってしまい、尿中Cl-が上昇して正確な原因診断(元々の発生・維持因子)を見誤る可能性があるためです。
代謝性アルカローシスの治療
1. 原因の除去
まずは、アルカローシスの原因となっている病態の除去を試みます。
- 消化管からの酸の喪失: 嘔吐による胃液の喪失であれば制吐薬を使用し、経鼻胃管によるドレナージが原因であれば、可能ならドレナージの終了を検討します。どうしてもドレナージを終了できない場合は、プロトンポンプ阻害薬(PPI)を投与して胃酸分泌を抑えH+の喪失を減らすアプローチも考慮されます。
- 利尿薬: 可能な限り原因となっている利尿薬(ループ利尿薬やサイアザイド系)の減量や中止を検討します。
2. ClとKの積極的な補充(尿Cl低下パターンの場合)
尿中Clが低下している状態では、腎臓がHCO3–を排泄できなくなっているため、輸液によるClの補充が不可欠です。また、代謝性アルカローシスは高頻度で低カリウム血症を合併(または悪化)させるため、Kの補充も同時に行う必要があります。
- 生理食塩液(0.9% NaCl)の投与: メインの輸液として生理食塩液を使用し、不足しているClと細胞外液量を補充します。
- 塩化カリウム(KCl)の混注: K補充とCl補充の両方の意味合いから、輸液へのKClの混注を積極的に行います。末梢静脈からの補正であれば、例えば「生理食塩液500mL + KCl 1キット(20mEq)」を患者の状態に合わせて40〜100mL/h程度で投与する方法が一般的です。
- 特殊な輸液の考慮: ナトリウム濃度に比べてCl濃度の高い「高カチオンギャップアミノ酸輸液(アミノレバン®など)」が有効であるという報告もあり、特に肝硬変患者の代謝性アルカローシスなどで意識的に使用されることがあります。
3. 生理食塩液が使えない場合(心不全など)の治療
心不全などでうっ血があり、生理食塩液による容量負荷がかけられず、かつ利尿薬の中止も難しいケースがあります。
- アセタゾラミド(ダイアモックス®)の投与: このような状況では、HCO3-の尿中排泄を促しながら利尿をかけることができるアセタゾラミドが極めて有用です。
- 注意点(K補充の徹底): アセタゾラミドを使用すると尿中へのK排泄が増加し、低カリウム血症が進行してアルカローシスの改善が妨げられることがよくあります。そのため、アセタゾラミドを使用する際は、積極的にKを補充しながら投与することが重要です。
補正を開始するタイミングについて
いつから補正を開始すべきかについての明確なコンセンサスはありませんが、一般的には動脈血pH > 7.55であれば積極的に補正すべきとされています。
参考文献
- Emmett M, Szerlip H. Causes of metabolic alkalosis. UpToDate. 2026 Apr 07.
- Kraut JA, Madias NE. Metabolic Acidosis of CKD: An Update. Am J Kidney Dis. 2016;67(2):307-317. doi:10.1053/j.ajkd.2015.08.028.
- Yi Y. Post-Hypercapnic Alkalosis: A Brief Review. Electrolyte Blood Press. 2023;21:18-23. doi:10.5049/EBP.2023.21.1.18.
- 柴﨑俊一. 3Rで整理する 輸液の基本の「き」 ~Redistribution:あえて代謝性アルカローシスを例に考える~. 民間医局コネクト. 2023 Jun 13.
- Emmett M, Szerlip H. Clinical manifestations and evaluation of metabolic alkalosis. UpToDate. 2026 Mar 17.
- 安田隆. 代謝性アルカローシス. medicina. 2018;55(7).
- 出口慧人, 玉井道裕. 代謝性アルカローシスの存在がわかった。では,その原因は?.INTENSIVIST 17巻1号




コメント