疫学
- 好発層: 患者の80〜90%以上が女性であり、特に閉経後の中高年女性(平均年齢67〜70歳)に圧倒的に多く発症します。
- 発症頻度: 急性冠症候群を疑われて受診した患者の約1〜2%(女性に限れば約10%)を占めており、決してまれな疾患ではありません。
- 誘因: 約3割は明確なストレスなく発症しますが、多くの場合、先行する精神的ストレス(身内の不幸、恐怖、極度の緊張、あるいは嬉しい出来事など)や、身体的ストレス(敗血症、手術、脳血管障害など)が引き金となります。
原因(病態生理・分子メカニズム)
明確な発症機序は完全に解明されていませんが、主に以下の要素が複雑に絡み合って発症すると考えられています。
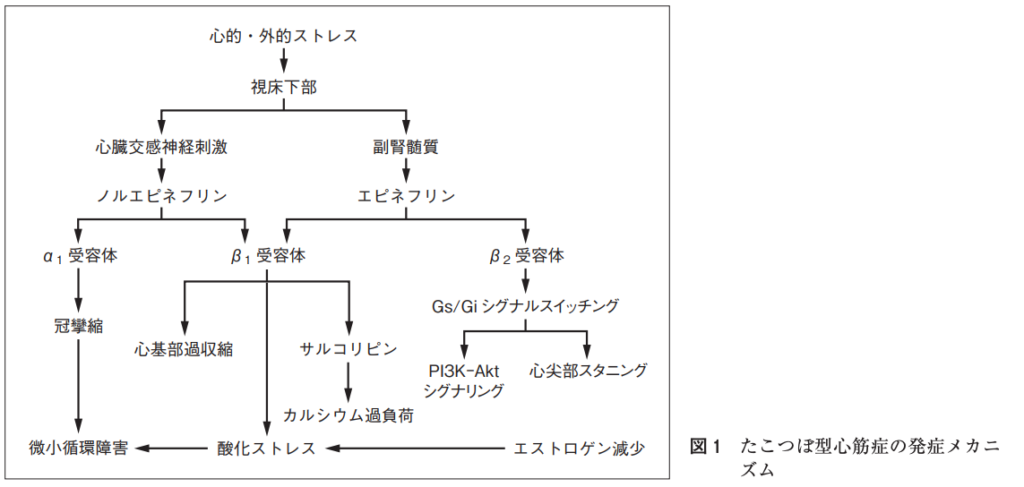
- カテコールアミンによる心筋障害(主因): 強いストレスにより交感神経が過剰に興奮し、血液中のカテコールアミン(アドレナリンなど)が急増します。心尖部には交感神経のβ2受容体が多く分布しており、過剰な刺激を受けると心筋を保護するために収縮を抑制するシグナル(Giシグナル)にスイッチし、心尖部の無収縮(気絶状態;スタニング)を引き起こします。一方、心基部には交感神経終末が多く分布しているため、過収縮をきたします。
- 微小循環障害: カテコールアミンの過剰により、心筋レベルの微小な血管が攣縮(スパスム)を起こし、一過性の血流低下を招きます。
- 修飾因子: エストロゲン(女性ホルモン)には心血管保護作用や血管拡張作用があるため、閉経によるエストロゲン低下が発症しやすさの基盤にあると考えられています。また、近年では扁桃体の過活動など「心脳連関(脳のストレス感受性)」の関与も指摘されています。
診断基準
国際的に広く用いられている最新の「InterTAK診断基準(2018年)」の要点は以下の通りです。

InterTAK 診断基準(2018年)」と「InterTAK Diagnostic Score(診断スコア)」の関係
「InterTAK 診断基準(2018年)」と「InterTAK Diagnostic Score(診断スコア)」は、どちらもたこつぼ症候群(TTS)を評価するための重要な指標ですが、臨床のプロセスにおける「目的」と「使われるタイミング」が異なります。
結論から言うと、診断スコアは初期段階で「確率を予測(スクリーニング)」するためのツールであり、診断基準は検査後に最終的な「確定診断」を下すためのルールという関係性にあります。
InterTAK Diagnostic Score(診断スコア)の役割:初期の「確率予測」
- 目的: 胸痛などで救急搬送された患者が、「たこつぼ症候群」なのか「急性冠症候群(ACS:急性心筋梗塞など)」なのかを、カテーテルなどの侵襲的な検査をする前に非侵襲的な項目で鑑別(スクリーニング)するためのツールです。
- 内容: 性別(女性)、ストレスの有無、精神・神経疾患の既往、心電図所見(aVR誘導以外のST低下の有無、QTc延長)といった7つの項目を点数化します。
- 使われ方: スコアが高いほどたこつぼ症候群の確率が高いと見積もります(例えば、心電図でST上昇がない場合、70点以上であれば「可能性大」、70点以下であれば「低〜中等度」と評価します)。この点数によって、次にどの検査(冠動脈CTや心エコー、あるいは緊急カテーテル検査)に進むべきかの方針決定に役立てます。
| 項目 | 点数 |
|---|---|
| 女性 | 25点 |
| 精神的ストレス | 24点 |
| 身体的ストレス | 13点 |
| aVR誘導以外でST低下を認めない(ST低下なし) | 12点 |
| 精神疾患(精神障害) | 11点 |
| 神経疾患(神経学的障害) | 9点 |
| QTc延長 | 6点(または8点)※ |
| 合計 | 100点 |
※文献により、QTc延長の点数を「6点」としているもの と、「8点」としているもの があります。
【スコアの解釈と目安】 合計スコアが大きくなるほど、たこつぼ症候群(TTS)である確率が上昇します。
- 40点: カットオフ値とした場合、TTSと急性冠症候群(ACS)の診断精度は感度89%、特異度91%となります。
- 50点以上: 95%以上の確率(感度94.7%)でTTSと診断できます。
- 31点以下: ACS診断の特異度が93.6%となり、ACSの可能性がより強く疑われます。
- アルゴリズム上の目安: 心電図でST上昇がない患者において、70点以上であれば「たこつぼ症候群の可能性大」、70点以下であれば「低〜中等度」として評価し、冠動脈CTなどの次の検査へ進む指標として用いられます。
InterTAK 診断基準(2018年)の役割:最終的な「確定診断」
- 目的: スコアで当たりをつけ、実際に心エコーやカテーテル検査などを行った結果を総合して、最終的にその患者を「たこつぼ症候群」として確定診断するための国際的な基準です。
- 内容: 「単一の冠動脈支配領域を超えた一過性の左室壁運動異常があるか」「急性心筋炎が除外できるか」といった必須条件が定められています。また、従来は除外されていた「褐色細胞腫」や「くも膜下出血などの神経疾患」が引き金となった場合(二次性たこつぼ症候群)も、この2018年の基準からは診断に含めることができるようになりました。
実際の臨床での関係性(診断のフロー)
これら2つは、以下のような流れで連携して使われます。
- 初期評価(スコアの使用): 胸痛や呼吸困難で患者が来院した際、特に心電図で明らかなST上昇がない場合などに、まず「InterTAK 診断スコア」を計算し、たこつぼ症候群の可能性を予測します。
- 検査の実施: スコアの予測や症状に基づき、心エコー(壁運動の確認)や、冠動脈CT・冠動脈造影(ACSの除外)などの画像検査を行います。
- 確定診断(診断基準の適用): すべての検査結果が出揃った段階で、その所見が**「InterTAK 診断基準(2018年)」**の項目を満たしているかを照らし合わせ、最終的にたこつぼ症候群と確定診断します。
つまり、「InterTAK Diagnostic Score」で疑いを強め、検査を行い、「InterTAK 診断基準(2018年)」で確定させる、という一連の診断プロセスを支える車の両輪のような関係にあります。
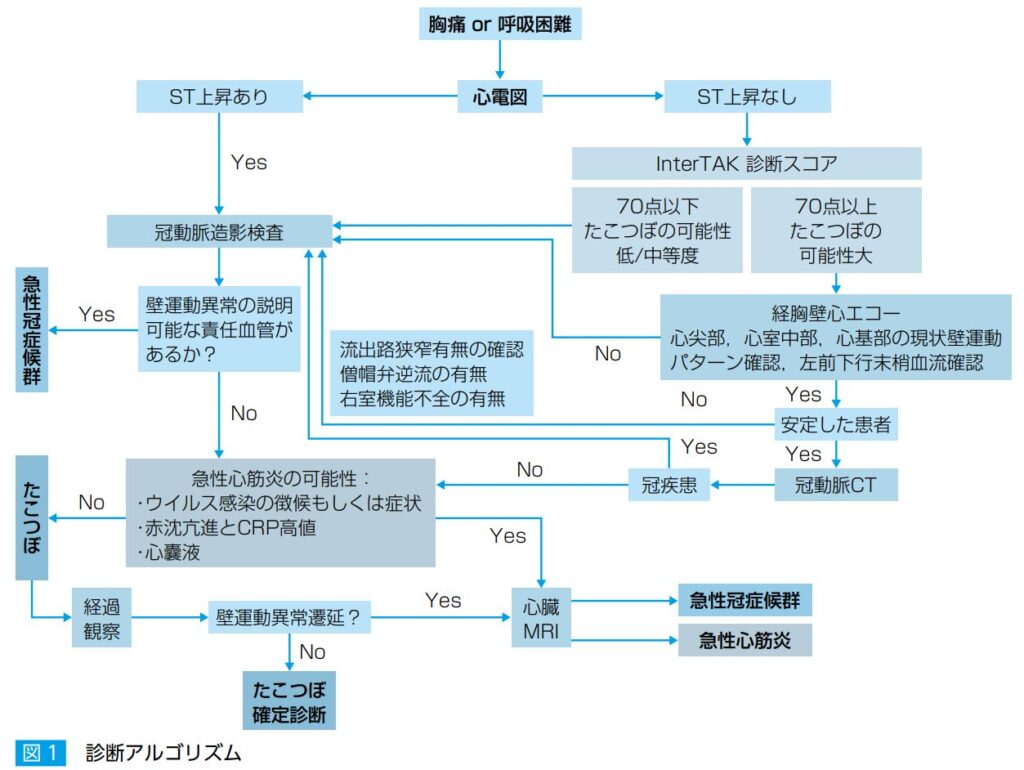
Mayo Clinic基準はなぜ使われなくなった?
初期のMayo Clinic基準(2004年版)がそのままの形では使われなくなり、新たな基準(InterTAK基準など)へと移行していった最大の理由は、Mayo Clinic基準が「非常に厳格な除外項目」を設けており、実際の臨床現場で遭遇する多様なたこつぼ症候群のケースを診断から弾いてしまっていたためです。
具体的には、以下のような変遷と背景があります。
■1. 初期のMayo Clinic基準(2004年)の厳格すぎる定義 2004年に提唱されたMayo Clinicの診断基準は、「最も厳格な『純粋なたこつぼ』の定義」と言えるものでした。この基準では、以下の状態を完全に「除外」していました。
- 閉塞性冠動脈疾患の合併
- 頭部外傷・頭蓋内出血などの神経疾患
- 褐色細胞腫
■2. 臨床像の多様性の判明と「心脳連関」の許容(2008年改訂) しかしその後、臨床像の多様性が明らかになるにつれ、脳卒中や頭部外傷などの急性期にたこつぼ症候群が合併するケースが数多く存在することが分かってきました。そのため、2008年の改訂版Mayo Clinic基準では、頭部外傷・頭蓋内出血が除外項目から削除され、神経疾患に合併するケース(心脳連関)も正式に診断可能となりました。
■3. より実臨床に即した「症候群」としての包括的基準へ(2016年〜現在) さらに研究が進むと、たこつぼ症候群は冠動脈疾患と共存しているケースや、褐色細胞腫に伴って発症するケースもあることが分かりました。 そのため、2016年のヨーロッパ心不全学会の基準や、現在の国際標準である「InterTAK診断基準(2018年)」では、Mayo Clinic基準の厳格な除外項目をさらに取り払い、「有意な冠動脈疾患があっても合併を容認する」「褐色細胞腫も二次性のたこつぼ症候群として包含する」といった形にアップデートされました。
このように、本疾患が単なる「心筋の障害」ではなく、多様な要因(特に脳や全身のストレス)が絡む「症候群(Takotsubo syndrome)」として広く捉えられるようになったため、厳格な除外を強いる古いMayo Clinic基準から、より実臨床に即した新しい基準へとシフトしていきました。
(※なお、現在でもUpToDateなどの一部の医学リソースや臨床現場では、改訂版のMayo Clinic基準が参照されることはありますが、国際的なトレンドとしてはInterTAK基準が主流となっています。)
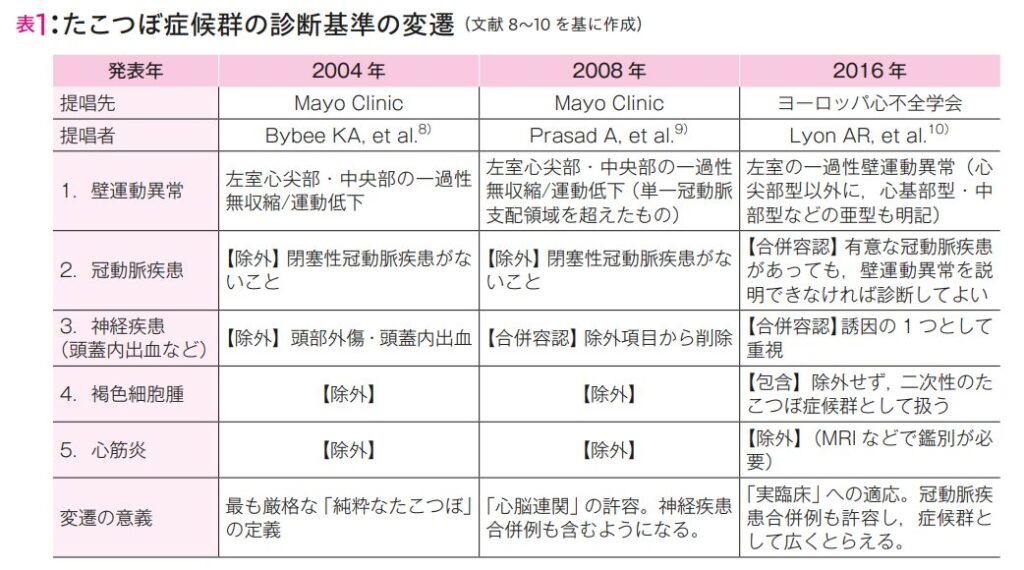
たこつぼ型心筋症の心電図
たこつぼ型心筋症(たこつぼ症候群)の心電図は、急性心筋梗塞(ACS)と非常に似た変化を示しますが、時期(超急性期〜亜急性期)によって特徴的な経時的変化をたどります。
ここでは、最も典型的な「心尖部型(Apical type)」の心電図特徴について詳しく解説します。
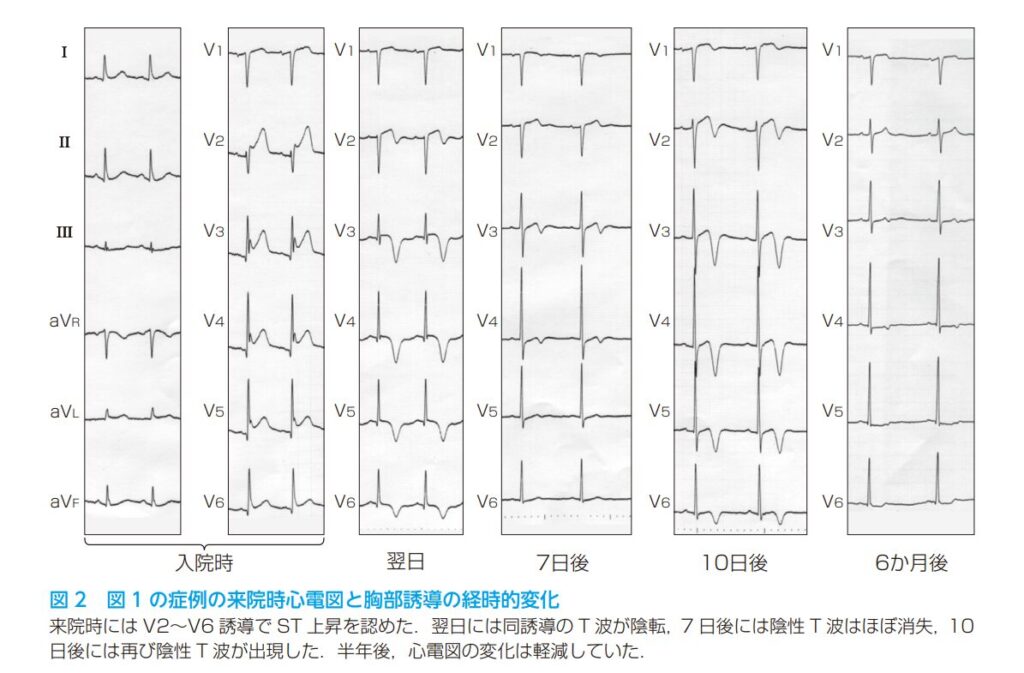
■超急性期(発症12時間以内)のST上昇
発症直後の超急性期には、左室心尖部の心筋障害を反映して、前胸部誘導(V2〜V5)や肢誘導(I、II誘導など)でST上昇を認めます。国際的なレジストリ研究では、患者の約43.7%にST上昇が見られました(Templin C et al.,Clinical Features and Outcomes of Takotsubo (Stress) Cardiomyopathy,N Engl J Med,2015年)。ただし、ACSと比較するとST上昇の程度は比較的軽度にとどまる傾向があります。一方で、ST低下で発症することは比較的まれ(約7.7%)です。
■亜急性期(発症2〜3日後以降)の巨大陰性T波
発症から2〜3日経つと、ST上昇はいったん基線に戻り、その後、広く深い「巨大陰性T波」が出現します。
- ピークと持続期間: 巨大陰性T波の形成は発症3日後と2〜3週間後にピークがあります。数ヶ月単位で持続した後に、多くは元の状態(正常)に戻ります。
- メカニズム: 心筋細胞そのものの障害というより、虚血に弱い「交感神経の脱落・障害」による再分極の遅延が原因と考えられています。交感神経が障害された領域が広範囲に及ぶため、多くの誘導で巨大陰性T波が見られます。
■急性心筋梗塞(ACS)との重要な鑑別ポイント
たこつぼ型心筋症と急性前壁心筋梗塞を心電図で鑑別する上で、以下の誘導の所見が非常に重要です。
- 「V1でST上昇なし」かつ「aVRでST低下あり」: たこつぼ型心筋症ではV1誘導でST上昇をきたす頻度は約6%と低く、逆に心尖部の対側性変化としてaVR誘導でST低下を認めます。この「V1でST上昇がなく、aVRでST低下がある」という所見は、感度90%以上(あるいは感度91%、特異度96%)という非常に高い精度で前壁中隔急性心筋梗塞と鑑別できるとされています。
- 下壁誘導での相反性変化がない: 急性前壁心筋梗塞では、心基部の虚血を反映して下壁誘導(II、III、aVF)でST低下(相反性変化)が起きます。しかし、たこつぼ型心筋症では心基部は過収縮しており、下壁誘導でのST低下は起きにくく、むしろ障害された心尖部を反映してST上昇の頻度が高くなります。
- 異常Q波は出現しにくい:急性心筋梗塞では心筋の壊死を示す「異常Q波」が出現しますが、たこつぼ型心筋症では心筋細胞は壊死しておらず一時的な「気絶心筋(stunning)」が主体であるため、異常Q波の出現頻度はACSに比べて少ないのが特徴です。
■著明なQT延長と致死性不整脈リスク
巨大陰性T波が出現するのと同じ時期(発症から48時間以内や2〜3日後)に、心筋の再分極遅延を反映して著明なQTc延長を伴うことが多いです。特にQT時間が500 msecを超えるような著明な延長はハイリスクとされ、トルサード・ド・ポアンツ(Torsades de pointes)などの致死性心室性不整脈を引き起こす危険性があるため、厳重な注意が必要です。
形態学的分類(壁運動異常のタイプ)
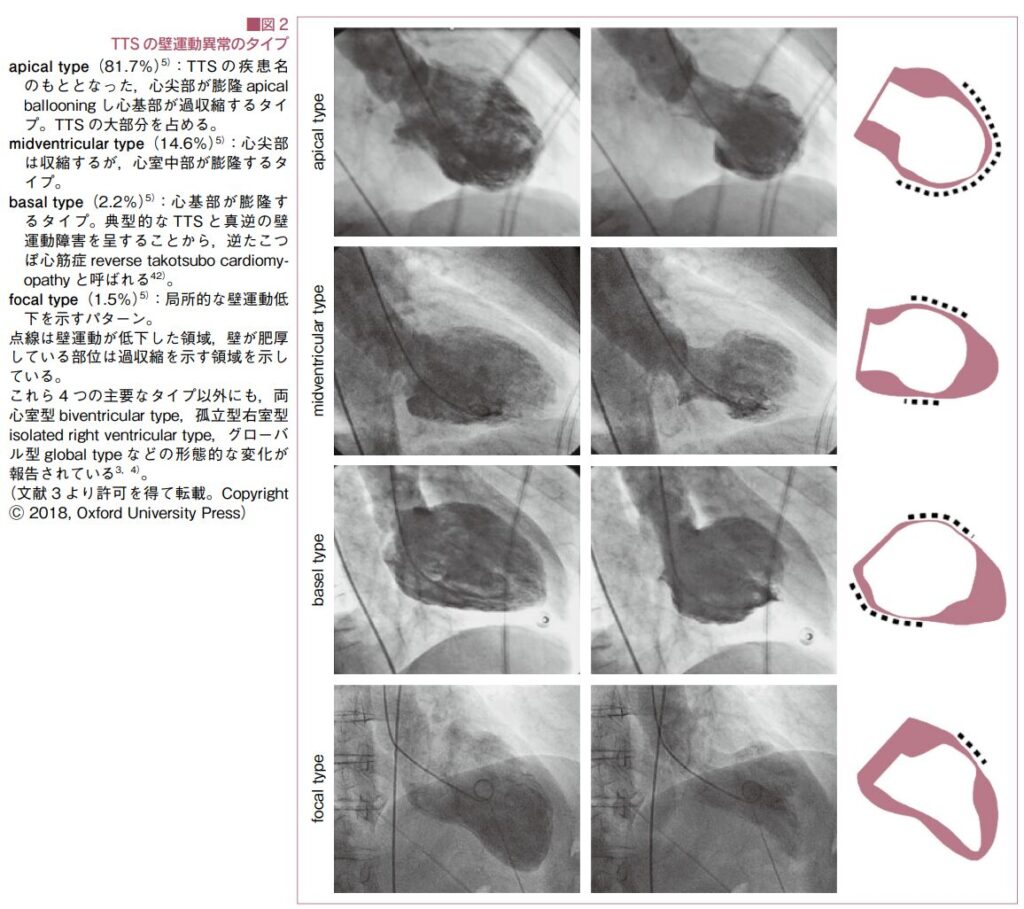
左室造影や心エコーで確認される壁運動異常のパターンは、大きく4つに分類されます。
- 心尖部型(Apical type):約81.7% 心尖部が風船のように膨らみ(無収縮)、心基部が過収縮する最も典型的なタイプ。まさに「蛸壺」の形を呈します。
- 心室中部型(Midventricular type):約14.6% 心尖部と心基部の収縮は保たれ、心室の中央部分のみが膨瘤するタイプ。
- 心基部型(Basal type):約2.2% 典型例とは真逆で、心基部が膨瘤し心尖部が過収縮する「逆たこつぼ型」。褐色細胞腫やクモ膜下出血に合併しやすいとされます。
- 局所型(Focal type):約1.5% 局所的な壁運動低下のみを示すタイプ。
治療
特異的な治療法は確立されておらず、急性期の合併症に対する支持療法・対症療法が基本となります。一過性の疾患であり、数週間で心機能は回復しますが、急性期に心不全や心原性ショックをきたすことがあり注意が必要です。
特に「左室流出路狭窄(LVOTO)の有無」で血圧低下時の対応が真逆になるのが最大のポイントです。
- 血行動態が安定している場合 一般的な心不全治療に準じて、β遮断薬やACE阻害薬/ARB、利尿薬などを使用します。
- ショック状態(血圧低下)に陥った場合
- LVOTOがない場合: カテコールアミン(強心薬)は病態を悪化させる懸念があるため使用を控えるべきですが、やむを得ない場合の一時使用や、大動脈内バルーンパンピング(IABP)、ECMO、IMPELLAなどの機械的補助循環が推奨されます。
- LVOTOを伴う場合(約10〜25%): 強心薬の投与や、利尿薬・血管拡張薬による前負荷の軽減(除水)は、狭窄をさらに悪化させるため禁忌です。治療には、補液による血管内ボリュームの維持、収縮力を抑えるβ遮断薬、血管収縮薬(フェニレフリンなど)が用いられます。
- その他の合併症と慢性期 心尖部に血栓が生じやすい(2〜8%)ため、血栓を認める場合や重度の機能低下がある場合はワルファリン等の抗凝固療法を少なくとも3ヶ月行います。慢性期の再発率(年間約1〜2%)を下げるためにACE阻害薬/ARBの継続が有効である可能性が示唆されていますが、確固たるエビデンスはまだありません。
たこつぼ型心筋症と左室流出路狭窄
疫学
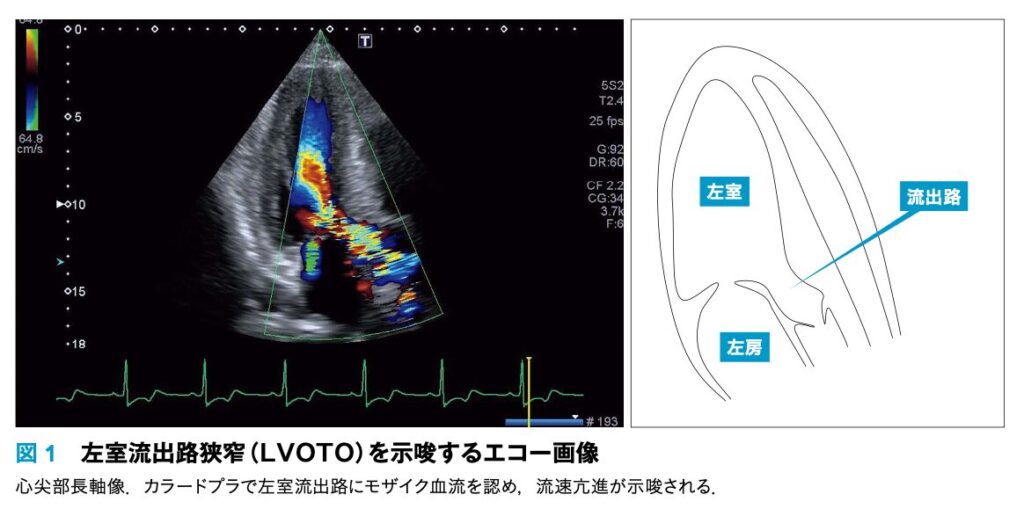
- 合併頻度: たこつぼ型心筋症の急性期にLVOTOを合併する頻度は、約12.8〜25%と報告されています。決してまれな合併症ではなく、日常診療でも十分に遭遇し得る確率です。
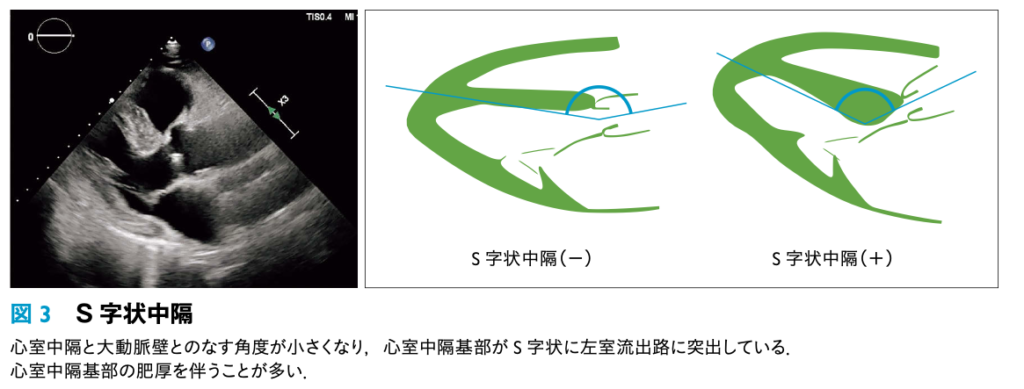
- 好発層: 高齢の女性に多く見られます。特に、加齢に伴って心室中隔基部が左室流出路に突出する「S状中隔(sigmoid septum)」を有する患者において、合併しやすいことが指摘されています。
2. 原因と発生メカニズム
なぜたこつぼ型心筋症でLVOTOが起きるのか、そのメカニズムは以下のステップで説明されます。
- ① 心基部の代償性過収縮: たこつぼ型心筋症の急性期には、心尖部から中間部にかけて広範な壁運動低下(無収縮)が生じます。これに対し、正常に動く心基部(basal portion)が心拍出量を補うように過剰に収縮(過収縮)します。
- ② 流出路の物理的狭小化と血流加速: この心基部の強い収縮によって、左室流出路が物理的に狭くなります。狭い部分を血液が無理に通過しようとするため、血流が急激に加速します。
- ③ ベンチュリ効果とSAMの誘発: 血流が加速することで陰圧が生じる「ベンチュリ効果(Venturi effect)」が働き、僧帽弁の前尖が流出路側に引き寄せられます。これがSAM(僧帽弁収縮期前方運動)です。
- ④ 閉塞の完成: SAMによって流出路の閉塞がさらに悪化し、同時に僧帽弁の接合不全が生じて急性僧帽弁逆流(MR)を引き起こします。
3. 「潜在的LVOTO」の顕在化(Latent LVOTO)
非常に重要な概念として、もともとS状中隔などがあり左室流出路が狭くなりやすい構造的素因(潜在的LVOTO)を持っている患者が、たこつぼ型心筋症による心基部の過収縮をきっかけとして、急性期に一気にLVOTOを顕在化させるというメカニズムが提唱されています。
4. 臨床的な影響と治療のピットフォール
- 重篤な合併症: LVOTOの合併は心拍出量を著しく低下させ、心原性ショックや心破裂といった破局的な状態(catastrophic outcomes)を引き起こす原因となります。今回の先生の症例がショックに至ったのも、まさにこのためです。
- 治療の注意点: 血圧が下がったからといって強心薬(カテコラミンなど)を投与したり、心不全に対して除水(利尿)を行って前負荷(心臓に戻る血液量)を減らしたりすると、心基部の過収縮がさらに強まり、流出路狭窄を悪化させてしまいます。治療には、収縮力を抑えて前負荷を増加させることで狭窄を解除するβ遮断薬が第一選択となります。
参考文献
- 「たこつぼ症候群(たこつぼ型心筋症)特集 虚血性心疾患:日常診療から専門医による治療まで」石原 正治,診断と治療 111巻 4号 pp. 531-535(2023年04月)
- 「たこつぼ症候群 特集 胸痛―見逃さない,間違えない 診断と専門医紹介のタイミング 緊急を要する胸痛:救急車で転送が必要な場合」明石 嘉浩,診断と治療 113巻 1号 pp. 57-61(2025年01月)
- 「ストレス性心筋症の生理学—たこつぼ症候群の臨床像とエビデンス 特集 生理学2Part 4 循環」出井 真史 , 野村 岳志,INTENSIVIST 14巻 2号 pp. 349-361(2022年04月)
- 「たこつぼ症候群:歴史的背景と最新事情 特集 心脳連関~脳と心臓・身体の不思議な関係~」明石 嘉浩,Heart View 30巻 5号 pp. 466-470(2026年05月)
- 「Current Opinion たこつぼ型心筋症」吉川 勉,呼吸と循環 61巻12号 ,pp.1160-1165,発行日 2013年12月15日
- 「新規の重症左室流出路狭窄」中坊 亜由美,臨床検査 vol.70 no.4 2026 年 4月・増大号



コメント